遺伝子変異に合わせたRNA標的創薬へ RNA構造と低分子化合物の相互作用を大規模に検出する新技術『BIVID-MaP』を開発
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | 個々の変異に最適化したRNA標的創薬と精密医療の実現への貢献が期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
最適化/突然変異/物質科学/遺伝情報/結合状態/cDNA/iPS細胞/がん関連遺伝子/体細胞変異/CD44/次世代シーケンサー/RNA/がん細胞/ラット/高次構造/創薬/低分子化合物/薬剤感受性/立体構造/がん患者/ゲノム/遺伝子/遺伝子発現/遺伝子変異/個別化医療/難病
2026年3月24日
/ 最終更新日時 :2026年3月24日
adiqb
RNP生命工学研究分野
京都大学iPS細胞研究所(CiRA)
株式会社xFOREST Therapeutics
東北大学
東京大学
科学技術振興機構(JST)
発表概要
【ポイント】〇RNA-低分子化合物相互作用の検出手法「BIVID-MaP」を開発しました
〇1塩基変異がRNA構造と結合能を変化させることを大規模に解明しました
〇個々の変異に最適化したRNA標的創薬と精密医療の実現への貢献が期待できます
要旨
宮下映見 大学院生(京都大学iPS細胞研究所(CiRA)未来生命科学開拓部門・株式会社xFOREST Therapeutics)、小松リチャード馨 最高技術責任者(株式会社xFOREST Therapeutics)、齊藤博英 教授(CiRA未来生命科学開拓部門・東京大学定量生命科学研究所)、および鬼塚和光 准教授(東北大学多元物質科学研究所)らの研究グループは、遺伝子変異によって変化するRNA構造と低分子化合物の相互作用を大規模に検出する新技術「BIVID-MaP」を開発し、変異特異的な化合物結合を1塩基レベルの解像度で特定することに成功しました。RNAの立体構造は、遺伝子発現を調節する重要な因子です。そのため、従来のタンパク質を標的とした手法ではアプローチが困難だった遺伝子を制御する、有望な創薬標的として注目されています。遺伝子の変異や個人間の遺伝的バリエーションはRNAの構造を変化させ、特定の低分子化合物に対する結合能(感受性)を左右することが知られています。しかし、これまで膨大な数の変異が低分子化合物との相互作用にどう影響するかを大規模に評価する手法は存在しませんでした。研究グループは、低分子化合物が標的RNAに結合した際に、そのRNA結合部位を化学修飾する「VQ(Vinyl-Quinazolinone)」ユニットと、逆転写注1反応時の塩基欠損を利用して結合部位を1塩基レベルの解像度で特定する「BIVID-MaP(Binding and VQ-induced Deletion-based Mutational Profiling)」法を構築しました(Fig. 1)。
この技術を用いて、代表的なRNA高次構造であるG4構造注2を対象に解析を行ったところ、G4構造の安定性や低分子化合物との結合状態を変化させる特定のがん変異の存在を明らかにしました。さらに、細胞溶解液という複雑な環境下においても、標的とするRNA構造への結合を正確に検出できることを実証しました。これらの成果は、個々の患者さんの遺伝的背景に基づいた「個別化医療」における、RNA標的創薬を加速させる強力なプラットフォームになることが期待されます。
この研究成果は2026年3月19日に「Nature Communications」で公開されました。
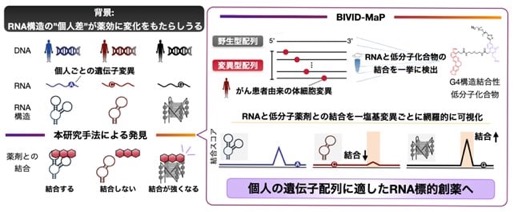
Fig. 1 本研究のまとめ
研究の背景
私たちの体の中で、RNAは単なる遺伝情報の伝達役にとどまらず、自ら複雑な立体構造を形作ることで、遺伝子の働きを精密にコントロールする重要な役割を担っています。近年、このRNAの立体構造を標的とした「RNA標的創薬注3」が、従来の薬では治療が難しかったがんや難病に対する画期的な治療法として世界中で大きな期待を集めています。特に、4本の鎖が絡み合った「G4構造」と呼ばれる特殊なRNA構造は、病気の原因となる遺伝子の制御に深く関わることが知られており、創薬の有力なターゲットとなっています。しかし、RNAを標的とする薬の開発には大きな課題がありました。それは、人それぞれの遺伝子のわずかな違い(バリアント)や、がん細胞で生じる突然変異です。RNAは非常に繊細で、配列の塩基がたった一つ入れ替わるだけで、その立体構造が劇的に変化したり、消滅したりしてしまいます。その結果、「ある患者さんにはよく効く薬が、別の患者さんの変異したRNAには全く結合せず、効果を発揮しない」という問題が起こり得ます。
これまで、膨大な数にのぼる変異RNAと低分子化合物との相性を、一つひとつ高精度かつ大規模に調べる手法は存在しませんでした。どの変異が化合物の結合を邪魔するのか、あるいは逆に結合を助けるのかを、1塩基レベルの細かい解像度で見極めることは非常に困難でした。
本研究は、この「遺伝子の多様性」と「薬の効き目」の複雑な関係を解き明かすためにスタートしました。患者さん一人ひとりの遺伝子配列に合わせた最適な薬を選ぶ「個別化医療」や、特定の変異を持つ細胞だけに狙い撃ちで作用する精密なRNA標的創薬を実現するための、全く新しい解析プラットフォームの構築を目指しています。
研究結果
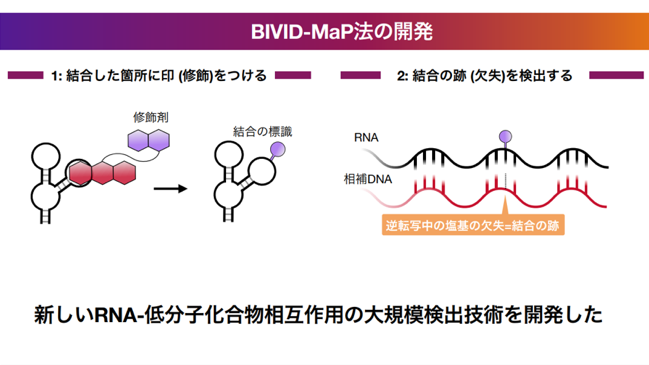
1)RNAと低分子化合物の「結合の跡」を読み取る技術「BIVID-MaP」RNAに「低分子化合物(Target RNA structure binding small molecule)」と「印を付けるユニット(VQ)」を合体させた化合物を反応させます。低分子化合物がRNAの特定の場所に結合すると、そのすぐ近くにある塩基にVQが「共有結合」という強い力で固定されます(Fig. 2)。本研究では、RNAの配列を写し取る反応(逆転写)を行うと、VQという特殊な「印」がある場所で読み取りがスキップされ、配列の一部が欠損する現象を発見しました。そして、この欠損した場所を次世代シーケンサー注4で解析することで、「欠損した場所≒化合物が結合した場所」として、1塩基レベルの非常に細かい精度で特定できることが示されました(Fig. 3)。
G4構造に結合する「Berberine」にVQを結合させた「Berberine-VQ」を作成しました。標的となるRNAにBerberine-VQを反応させて、逆転写して得られたDNAを次世代シーケンサーで解析し、どの塩基にBerberineが結合していたかを特定すると、G4構造に結合していました。つまり、BIVID-MaPはRNAと低分子化合物が相互作用する部位を特定できることを表しています。
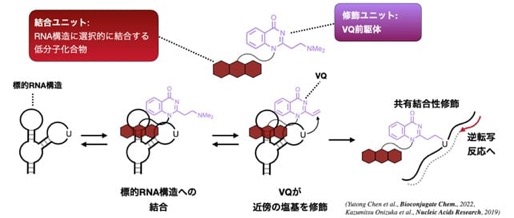
Fig. 2 特定のRNA構造を修飾する工程
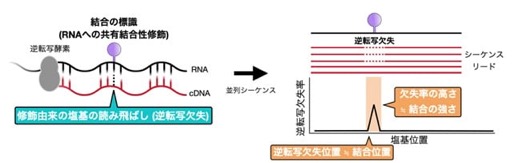
Fig. 3 逆転写により低分子化合物が結合していたRNAの領域を推定する工程
2)遺伝子のわずかな個人差が薬の効き目を変えることを解明
次に1箇所の変異が、化合物とRNAの結合にどのような影響を与えるかを調査しました。標的となるRNA配列(CD44 I8野生型)に対して、1塩基置換を導入した変異型(CD44 I8変異型)を合成しました。このRNAに対して「BIVID-MaP」を利用し、Berberineとの相互作用を測定しました。
野生型のRNAでは高い頻度で「結合の跡(欠損)」が検出されたのに対し、変異型ではその跡が激減しました(Fig. 4)。これは、たった一つの変異によってRNAの立体構造が崩れ、Berberineが結合できなくなったことを示しています。このように、個人の持つ変異に合わせて効く薬を判定できることが示されました。
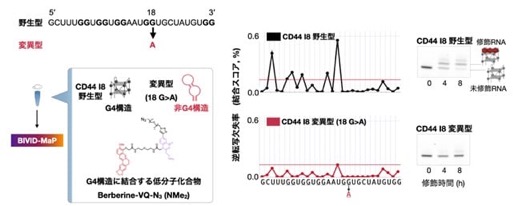
Fig. 4 BIVID-MaPによるG4構造へのBerberineの結合評価
3)遺伝子変異による “薬の効き目”の大規模検出
次に、実際のヒトの遺伝子データを用いて、変異が “薬の効き目” にどう影響するかを大規模に検証しました。そこで、がん分野での医薬応用が待望されている「5’UTR(タンパク質の合成を調節する領域)」のG4構造に着目しました。まず、ヒトのゲノムデータから5’UTRを持つ「がん関連遺伝子」を抽出しました。そして、これらの正常な配列(野生型)に加えて、データベース(COSMIC)に登録されている「がん患者さん由来の変異(がん体細胞変異)」を含む、1,600種類以上に及ぶRNAライブラリを作成しました (Fig. 5)。この大規模なRNAライブラリに対してBerberine-VQを反応させ、どの変異がBerberineとの結合を強めるか、あるいは弱めるかを一挙に測定しました。
その結果、わずか1塩基の変異によって、Berberineが結合しなくなるだけでなく、逆に野生型よりも強く結合するようになる「変異特異的な相互作用」が多数存在することを明らかにしました(Fig. 6)。
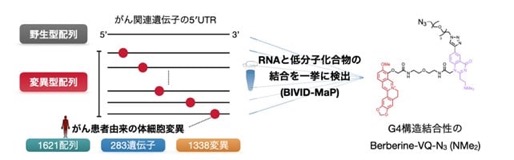
Fig. 5 ヒトがん体細胞変異5’UTR群とBerberine結合の大規模検出
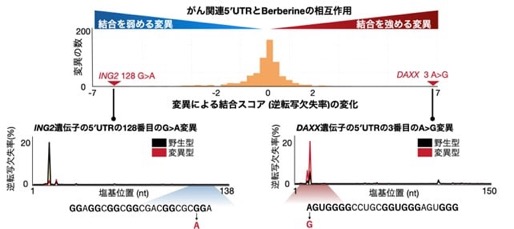
Fig. 6 Berberineと5’UTR内配列との結合を変化させてしまうがん関連変異の発見
まとめと展望
本研究により、RNA構造と低分子化合物の相互作用を1塩基レベルの解像度で大規模に検出する新技術「BIVID-MaP」を確立しました。化合物結合部位を化学的に標識し、逆転写反応の欠損として検出することで、特定の遺伝子変異がRNAの立体構造や薬剤感受性に与える影響を正確に捉えることに成功しました。細胞溶解液内という複雑な環境下でもその有効性が実証された点は、実用化に向けた大きな成果です。今後の展望として、本技術は「個別化医療」の推進に大きく貢献します。患者さん個々のバリアントに応じた最適な薬剤選定や、疾患特有の変異を標的とする精密なRNA標的創薬が可能になります。また、将来的には生きた細胞内での挙動解析への応用も見込まれ、未だ治療法の乏しい難病に対する新たなアプローチを提供する、次世代の創薬プラットフォームとしての役割が期待されます。
本研究への支援
本研究は、以下の支援を受けて実施されました。〇日本学術振興会(JSPS)
― 科学研究費助成事業 (JP20H05626、JP25H00970、JP23KJ1331、JP23H02076、JP24K01641)
〇科学技術振興機構(JST)
― 戦略的創造研究推進事業CREST(JPMJCR23B3)
― 創発的研究支援事業(JPMJFR2002)
〇京都大学iPS細胞研究基金
用語解説
注1) 逆転写RNAを型としてDNA(cDNA)を合成する反応。本研究では、VQによる「印」がある場所でこの反応が止まったりスキップしたりする性質を利用し、化合物の結合場所を配列データ上の「欠損」として特定する。
注2) G4構造(G-quadruplex)
グアニン(G)が豊富なRNA配列が形作る、4本鎖の特殊な立体構造。病気の原因となる遺伝子の制御に深く関わっているため、創薬における有力なターゲットとなっている。
注3) RNA標的創薬
従来の医薬品が主にタンパク質を標的としていたのに対し、疾患に関与するRNAそのものを標的とする新しい創薬手法。これまで治療が難しかったがんや難病に対する画期的な治療法として期待されている。
注4) 次世代シーケンサー
膨大な数の核酸配列を同時並行で高速に読み取ることができる装置。本手法では、この技術を用いることで、どの塩基に化合物が結合していたかを網羅的かつ高精度に解析する。
アイキャッチ画像
雑誌名等
雑誌名:Nature Communications題 名:Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes
著者名:Emi Miyashita1,2, Kazumitsu Onizuka3*, Yutong Chen3, Hiroki Yoshida2, Hina Hatayama3, Shunya Ishikawa3, Peijie Yan2, 4, Takahito Hasegawa3, Mamiko Ozawa3, Kaho Maeta2, Fumi Nagatsugi3, Hirohide Saito1,4*, Kaoru R. Komatsu2*
*責任著者
著者の所属機関:
1.京都大学 iPS細胞研究所(CiRA)
2.株式会社xFOREST Therapeutics
3.東北大学 多元物質科学研究所
4.東京大学 定量生命科学研究所
DOI:https://www.doi.org/10.1038/s41467-026-70097-9
問い合わせ先
東京大学定量生命科学研究所 総務チームTel:03-5841-7813 E-mail:soumu@iqb.u-tokyo.ac.jp
 東京大学 研究
東京大学 研究