転写中にヌクレオソームに化学修飾を導入する機構を解明
――RNA ポリメラーゼ II はヌクレオソームを通過中に修飾する――
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | エピジェネティクスの分子・構造基盤情報を提供するとともに、クロマチンや転写制御の破綻による疾患メカニズムの解明への貢献が期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
画像処理/閉じ込め/構造形成/電子線/ヒストン/極低温/電子顕微鏡/転写伸長/ヌクレオソーム/構造変換/クロマチン構造/クライオ電子顕微鏡/ヒストンシャペロン/シャペロン/クロマチン/ヒストンメチル化/ヒストンメチル化酵素/分子機構/RNA/アセチル化/アミノ酸/イミン/ヒストン修飾/メチル化/遺伝子発現制御/構造生物学/構造変化/細胞核/細胞生物学/創薬/転写制御/発現制御/立体構造/立体構造解析/がん患者/ゲノム/遺伝子/遺伝子発現
2026年1月29日
/ 最終更新日時 :2026年1月29日
adiqb
クロマチン構造機能研究分野
東京大学理化学研究所
発表のポイント
◆遺伝子を読み取る酵素「RNA ポリメラーゼ II」が、転写の障壁となる「ヌクレオソーム」を解体した後、正常な遺伝子発現の維持に不可欠なヌクレオソームのメチル化修飾(H3K36me3)が再構築する過程において導入されることを発見しました。◆クライオ電子顕微鏡解析により、ヌクレオソームのメチル化酵素「Set2」が RNA ポリメラーゼ II に直接結合し、再構築されたヌクレオソームへ修飾を導入する様子の可視化に成功しました。これにより、転写過程における Set2 の作動機構が明らかになりました。
◆本研究は、DNA 配列の変化を伴わない遺伝子発現制御「エピジェネティクス」の分子・構造基盤とともに、メチル化の異常に起因するがん等の疾患理解や、創薬に向けた知見を提供します。
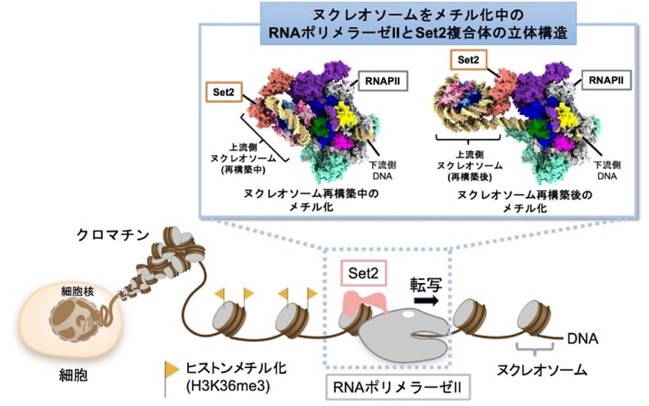
RNA ポリメラーゼ II による転写に伴うヒストンメチル化酵素 Set2 によるヒストンメチル化
発表内容
東京大学定量生命科学研究所の鯨井智也講師、胡桃坂仁志教授、大屋恵梨子助教、小林武彦教授、理化学研究所(理研)生命医科学研究センター転写制御構造生物学研究チームの江原晴彦上級研究員、関根俊一チームディレクター(兼:生命機能科学研究センター 構造生命科学/細胞生物学連携チーム 上級研究員)らの共同研究グループは、遺伝子発現を担う「RNA ポリメラーゼ II(RNAPII)」(注 1)が、転写に伴い解体されたヌクレオソーム(注 2)を再構築する過程で、ヌクレオソームを構成するヒストン H3 にメチル化(注 3)修飾(H3K36me3)を導入する仕組みの詳細を解明しました。この修飾は、正常なクロマチン構造(注 4)や遺伝子発現を維持する役割を果たします。本成果は、エピジェネティクス(注 5)の分子・構造基盤情報を提供するとともに、クロマチンや転写制御の破綻による疾患メカニズムの解明への貢献が期待されます。<研究背景>
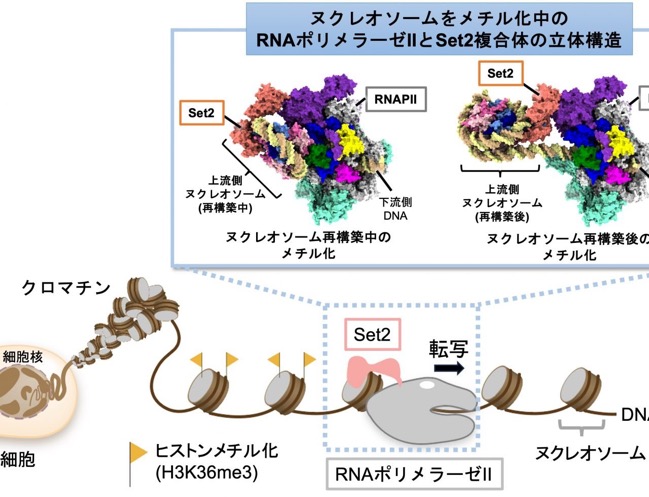
ヒトを含む真核生物において、遺伝子の読み取り装置 RNA ポリメラーゼ II(以下、RNAPII)はゲノム DNA を転写する主要な酵素であり、メッセンジャーRNA を合成するという遺伝子発現の根幹を担っています。細胞核の内部に収納されたゲノム DNA は、ヒストンタンパク質に DNAが巻き付いた「ヌクレオソーム」と呼ばれる糸巻きのような構造が、数珠状に連なったクロマチン構造をとっています。しかし、ヌクレオソームは RNAPII にとっては、進行を阻む「壁」となります (図 1) 。
共同研究グループはこれまで、RNAPII がヌクレオソームを通過する様子を、クライオ電子顕微鏡を用いた立体構造解析(注 6)により可視化してきました。その結果、RNAPII が様々な転写伸長因子(注 7)と共に転写伸長複合体(以下、EC)を形成し、進行方向(下流)のヌクレオソームを解体して通過した後、後方(上流)で再構築するメカニズムを解明しました(https://www.riken.jp/press/2022/20220819_1/index.html)。 また、その過程で、RNAPIIがヌクレオソームの DNA を剥がして解体すると、ヒストンシャペロン(注 8)「FACT」(以下、FACT)がヒストンに結合し、RNAPII の上流での再構築を補助することを明らかにしていまし
た。
他方、細胞内の活発に転写されている領域では、ヒストンのメチル化酵素「Set2」(酵母の遺伝子。ヒトでは「SETD2」というタンパク質が同様の活性を持つ。) (以下、Set2)により、「ヒストンメチル化(H3K36me3:ヒストン H3 の 36 番目のリシンのトリメチル化)」が導入されています(図 1)。この修飾は、活発に転写されている遺伝子領域の目印となるとともに、正常なクロマチン構造を保ち、異常な転写を抑制すると考えられています。これまで、このメチル化はRNAPII による転写に伴って導入されると考えられていました。しかし、転写の過程ではヌクレオソームは解体され、そして再構築されるという、非常にダイナミックな構造変換が起こります。このような激しい構造変換の中で、ヒストンのメチル化の具体的な導入プロセスは不明でした。
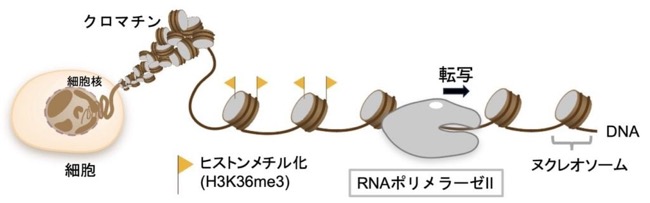
図 1. クロマチンにおける RNAPII の転写の概念図。
<研究内容>
今回、共同研究グループはこれまでに確立した EC(転写中の RNAPII と転写伸長因子 Spt6、Spt4/5、Elf1、Spn1、Paf1C との複合体)と FACT によるヌクレオソーム転写の試験管内実験系を用いて、Set2 が転写中にヒストンにメチル化を導入するメカニズムを調べました。実験ではまず、ヌクレオソームから離れたところから転写を開始させ、EC がヌクレオソームを通過する前後でのメチル化を解析しました(図 2A)。その結果、転写が行われることでメチル化の効率が大きく向上することを発見しました。そこで、Set2 がヌクレオソーム通過のどのタイミングで修飾を行うのかを詳細に調べるため、DNA 配列に細工をすることで、EC をヌクレオソーム上の様々な位置で停止させ、ヌクレオソームが EC の下流に存在する場合、および、上流に存在する場合でのメチル化を解析しました(図 2B)。その結果、主に EC がヌクレオソームを解体した後に、上流に再構築されたときにメチル化が導入されることが明らかになりました。さらに、ヌクレオソームが EC の下流側に存在する場合には、ヌクレオソームの解体・再構築を補助するFACT がヌクレオソームに結合し、Set2 によりメチル化が導入されないよう制御していることも判明しました。これにより、EC が通過したヌクレオソームのみ、つまり、転写された領域だけに正確にメチル化が導入される制御機構が示唆されました。
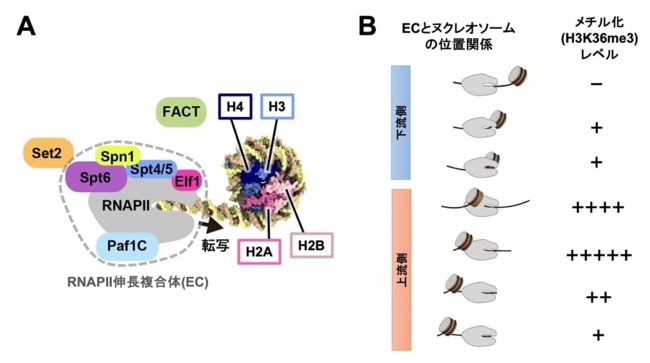
図 2.転写に伴うヒストンメチル化実験。
(A)RNAPII 伸長複合体(EC)によるヌクレオソーム転写実験の概念図。EC は、転写中の RNAPII に転写伸長因子 Spt6、Spt4/5、Elf1、Paf1C、Elf1、Spn1 が結合している。
(B)EC をさまざまな位置で停止させたときのメチル化アッセイ。ヌクレオソームが EC の上流側に位置するときに、メチル化が顕著に上昇する。
次に、このメカニズムを構造的に解明するため、メチル化反応中の「EC・ヌクレオソーム・Set2」複合体について、クライオ電子顕微鏡を用いた立体構造解析を行いました。その結果、EC の上流側でヌクレオソームが再構築されている途中の状態(図 3A)、および、再構築が完了した状態(図 3B)の、2 つの状態で Set2 がヌクレオソームに結合している様子を捉えることに成功しました。いずれの構造においても、Set2 はヒストンのメチル化を行う体制となっていました。興味深いことに、Set2 は EC を構成する転写伸長因子「Spt6」とも結合していました(図 3、赤丸で図示)。この結合により、Set2 は上流側のヌクレオソームに近い位置に固定され、効率的にメチル化を行える配置となっていました。2 つの構造を比較したところ、Set2 は柔軟に構造を変化させることができ、これにより再構築されたヌクレオソーム内の 2 つのヒストン H3 タンパク質の双方に修飾を導入できることも明らかになりました。また、この Set2 の Spt6 結合部位は、酵母からヒトに至るまで高度に保存されていました。そして、試験管内の実験だけでなく、生きた酵母のなかでも Set2 の Spt6 への結合が、メチル化のために重要であることも確認されました。
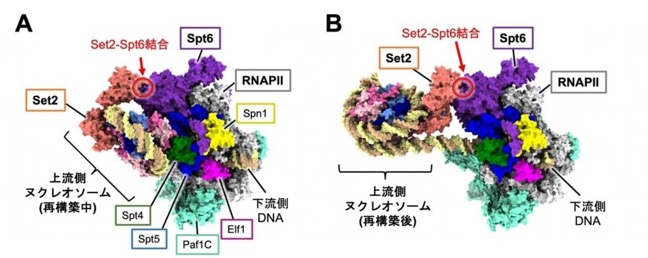
図 3. 本研究で明らかになった EC-ヌクレオソーム-Set2 複合体構造。(A)再構築中のヌクレオソームに Set2が結合している複合体構造。(B) 再構築後のヌクレオソームに Set2 が結合している複合体構造。
以上の今回の結果とこれまでの研究の知見を総合して、ヌクレオソーム転写におけるヒストンメチル化のモデルを提唱しました(図 4)。まず、EC が下流側のヌクレオソームに衝突して DNAを剥がすことでヌクレオソームの解体を開始します(図 4、ステップ 1)。ヌクレオソームの DNAが剥がされたことを FACT が検知して結合します。このとき、FACT の結合により下流側ヌクレオソームへの Set2 によるメチル化が抑制されます。さらに EC が進行すると、FACT-ヒストンの複合体が EC の上流側に転移します(図 4、ステップ 2)。ヌクレオソームの再構築が開始されると FACT が解離し、Set2 がヌクレオソームにアクセスしてメチル化を導入します(図 4、ステップ 3)。EC の進行に伴い、一度 Set2 はヌクレオソームから解離してヌクレオソームの再構築が進みます(図 4、ステップ 4)。ヌクレオソーム再構築完了後に、Set2 が柔軟に構造変化することで、もう一度メチル化を導入します(図 4、ステップ 5)。これにより、ヌクレオソームの転写に伴い、2 つのヒストン H3 にメチル化が導入されると考えられます(図 4、ステップ 6)。
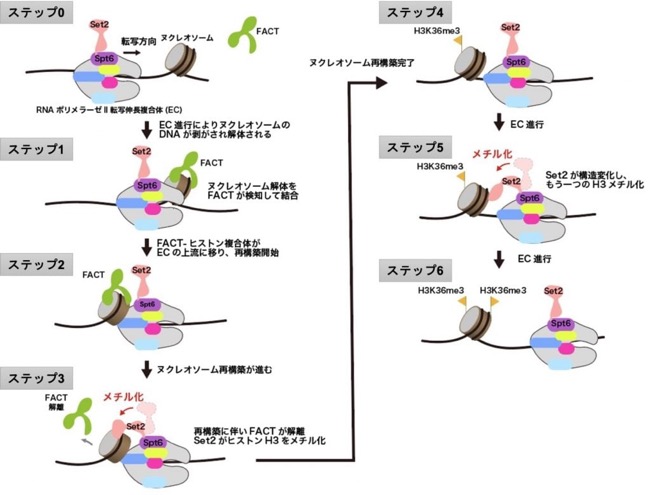
図 4. 本研究で提案する EC のヌクレオソーム転写に伴うヒストンメチル化機構。
<今後の展望>
本研究では、EC がヌクレオソームを通過する際の立体構造を可視化することで、転写過程におけるヒストンメチル化導入の分子機構の詳細を解明しました。これは、遺伝子発現中のクロマチン構造形成に関する理解を深める重要な知見です。近年、ヒストン修飾の異常、つまりエピゲノム異常による遺伝子発現制御の破綻が、がんの原因となることが報告されています。実際に、本研究の対象である Set2(酵母のタンパク質)のヒト版タンパク質「SETD2」は、がんとの関連が指摘されています。興味深いことに、ヒト SETD2 においてヒト版転写伸長因子「SPT6」との結合を担うと想定される部位には、一部のがん患者で変異が見つかりました。当該変異がヒストンメチル化の異常を引き起こし、正常な遺伝子発現制御が破綻したためにがんにつながった可能性が考えられます。本成果は、クロマチンおよび転写関連因子の構造・機能の解明研究を前進させ、がんをはじめとする様々な疾患の原因究明や、創薬への貢献が期待されます。
研究助成
本研究は、日本学術振興会(JSPS)の科研費(課題番号:JP20H05690、JP24H00062、JP20H03201、JP23K17392、JP22K15033、JP24H02328、JP23H05475、JP20H05906、JP21H04761、JP20K15772、JP25K18404)、科学技術振興機構(JST)の戦略的創造研究推進事業 ERATO(課題番号:JPMJER1901)、CREST(課題番号:JPMJCR24T3、JPMJCR19S3)、日本医療研究開発機構(AMED)の生命科学・創薬研究支援基盤事業(BINDS)(課題番号:JP25ama121009)の支援により実施されました。用語解説
(注 1)RNA ポリメラーゼ II(RNAPⅡ)DNA を鋳型にして、RNA を合成することを転写といい、RNA ポリメラーゼはこの反応を行う。ヒトの RNA ポリメラーゼには 3 種類あり、RNA ポリメラーゼ II は遺伝子をコードするゲノム DNA領域を転写し、メッセンジャーRNA を合成する。他の RNA ポリメラーゼ(I および III)は、主に遺伝子以外の特定の DNA 領域を転写する。
(注 2)ヌクレオソーム
4 種類のヒストンタンパク質 H2A、H2B、H3、H4 が 2 分子ずつ組み合わさったヒストンの 8量体にDNA が巻き付いた円盤状の構造体。ヌクレオソームがいくつも連なる数珠状構造を骨格としてクロマチンが形成されている。
(注 3)メチル化
タンパク質の中のアミノ酸にメチル基(-CH3)を付加する反応。メチル化酵素は、この反応を触媒する。メチル基が導入されたアミノ酸は、メチル化を認識するタンパク質の結合を促進する役割を果たすシグナルとして機能する。
(注 4)クロマチン構造
酵母からヒトなどの生き物のゲノム DNA は、ヒストンタンパク質に巻き付いて細胞の核内に収納されており、数珠状の構造を取っている。この数珠状構造には多種多様なタンパク質が結合しており、その巨大な複合体を「クロマチン」と呼ぶ。クロマチン構造は長大な DNA を効率よく収納するだけでなく、その構造の変換を通して遺伝子の働きを制御している。
(注 5)エピジェネティクス
DNA 配列の変化を伴わない遺伝子発現変化の仕組みの研究分野。ヌクレオソームに含まれるヒストンのメチル化、アセチル化などの化学修飾や、DNA のメチル化などのエピゲノムと呼ばれる因子により、遺伝子発現は制御されている。「エピ」のない「ジェネティクス」は、DNA配列にコードされた遺伝子の研究分野のこと。
(注 6)クライオ電子顕微鏡を用いた立体構造解析
クライオ電子顕微鏡は、タンパク質などの試料を非結晶の氷の中に閉じ込め、極低温下(-180℃)で電子線を用いて高解像度の画像を取得する装置。タンパク質 1 分子ずつについて、さまざまな方向を向いた分子の画像を収集し、画像処理と組み合わせることによって、高解像度の 3 次元立体構造を決定する。
(注 7)転写伸長因子
RNA ポリメラーゼ II に結合して、転写伸長反応を助ける因子。RNA ポリメラーゼ II の転写には大きくわけて開始、伸長、終結の 3 つのフェーズがある。転写伸長因子は、伸長のステップで機能する。転写伸長因子には、Spt6, Spt5, Spt4, Elf1, Spn1, Paf1C など多数の種類が存在する。
(注 8)ヒストンシャペロン
ヒストンタンパク質に結合してヌクレオソームの崩壊や構築を補助する因子の総称。ヒストンシャペロン FACT は、ヌクレオソームから一部 DNA が剥がれた状態に結合して、崩壊や再構築を補助する。「シャペロン」は、タンパク質の構築を補助する因子を示す。
アイキャッチ画像
雑誌名等
雑誌名:Science Advances題 名:Structural basis of transcription-coupled H3K36 trimethylation by Set2 in
coordination with FACT
著者名: Tomoya Kujirai(鯨井智也)†, Haruhiko Ehara(江原晴彦)†, Tomoko Ito(伊藤
友子), Masami Henmi(邉見真生), Eriko Oya(大屋恵梨子), Takehiko Kobayashi
(小林武彦), Shun-ichi Sekine (関根俊一) *, Hitoshi Kurumizaka(胡桃坂仁志)
*【†:共同筆頭著者、*:責任著者】
DOI:10.1126/sciadv.aed1952
URL:https://www.science.org/doi/10.1126/sciadv.aed1952
問い合わせ先
(研究内容については発表者にお問合せください)東京大学定量生命科学研究所
教授 胡桃坂 仁志(くるみざか ひとし)
Tel:03-5841-1467 E-mail:kurumizaka @ iqb.u-tokyo.ac.jp
東京大学定量生命科学研究所 総務チーム
Tel:03-5841-7813 E-mail:soumu @ iqb.u-tokyo.ac.jp
理化学研究所 生命医科学研究センター
チームディレクター 関根 俊一 (せきね しゅんいち)
Tel:045-503-9257 E-mail:shunichi.sekine @ riken.jp
理化学研究所 広報部 報道担当
Tel:050-3495-0247 E-mail:ex-press @ ml.riken.jp
 東京大学 研究
東京大学 研究