細菌の「遺伝子運び屋」、プラスミドが持つ「生存戦略」を発見
ー薬剤耐性拡散のパターンが明らかにー
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | 薬剤耐性遺伝子拡散の段階を判断する簡便な指標を提供するだけでなく、将来的には初期拡散を担うプラスミドを標的とした新たな拡散防止戦略の構築に貢献することが期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
普遍性/ゲノムDNA/生存戦略/CRISPR-Cas/古細菌/接合伝達/プラスミド/生態学/微生物/転写抑制/免疫系/CRISPR/腸内環境/イミン/ストレス応答/ファージ/ゲノム/ストレス/遺伝子/遺伝子発現/細菌/腸内細菌/薬剤耐性
DATE2026.01.23#Press Releases
発表のポイント
細菌間を移動する「遺伝子の運び屋」であるプラスミドのうち、多様な細菌を宿主とできる広宿主域プラスミドとそうでない狭宿主域プラスミドが、それぞれ特徴的な遺伝子を持ち、異なる「生存戦略」をとっていることを発見した。新たに提唱したプラスミド生存戦略の概念に基づき、薬剤耐性遺伝子の初期拡散が特定の生存戦略をとるプラスミドによって媒介されやすいというパターンを発見し、「ステルス・ファースト」モデルと命名した。
本成果は、薬剤耐性遺伝子拡散の段階を判断する簡便な指標を提供するだけでなく、将来的には初期拡散を担うプラスミドを標的とした新たな拡散防止戦略の構築に貢献することが期待できる。
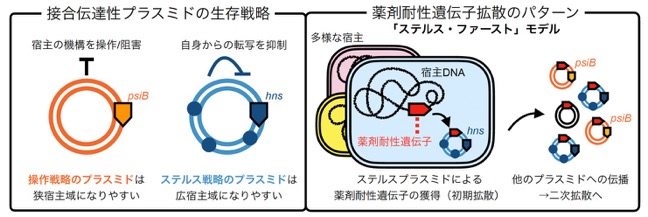
提唱した接合伝達性プラスミドの生存戦略とそれらの宿主域・薬剤耐性伝播との関係
発表概要
カリフォルニア大学バークレー校比較生化学専攻の小野隆一大学院生と東京大学大学院理学系研究科の今野直輝客員共同研究員、古澤力教授らによる研究チームは、微生物が持つ薬剤耐性遺伝子を媒介することで知られる接合伝達性プラスミド(注1 ,注2 )のDNA配列情報を解析し、多様な系統の種に伝播する広宿主域プラスミドと特定の系統のみに伝播する狭宿主域プラスミドが持つ遺伝子セットの違いを絞り込みました。その結果、広宿主域のプラスミドが自身の遺伝子の発現を抑えて宿主の負担を下げる機能の遺伝子を持つ一方で、狭宿主域プラスミドは宿主の機構を積極的に操作/阻害する遺伝子を持つ傾向を発見しました。これらの性質は生物の生存戦略になぞらえてそれぞれ「ステルス戦略」と「操作戦略」と命名されました。さらに、世界中で課題となっている薬剤耐性遺伝子の拡散プロセスにおいて、ステルス戦略を持つプラスミドが先に薬剤耐性遺伝子の初期拡散を担い、数年後に他のプラスミドが二次拡散を担う傾向を発見し、「ステルス・ファースト」モデルとして提唱しました。この成果は、多様な薬剤耐性遺伝子の各々が拡散のどの段階にあるかを判断する簡便な指標となり、将来的には初期拡散を担うプラスミドを標的とした新たな拡散防止戦略の構築に貢献することが期待されます。発表内容
地球上にはさまざまな微生物が存在します。その中でも細菌や古細菌と呼ばれる微生物はしばしばゲノムDNAと独立した環状DNAであるプラスミドを持ちます。主に親から子へのみ垂直に受け継がれるゲノムDNAと対照的に、プラスミドは親子関係にない個体間で、時には種の垣根さえ越えて水平に移動し拡散することが知られています。これに伴う遺伝子の水平伝播は細菌・古細菌の高速な進化を可能にする一つの要因であるとともに、現在世界的な問題となっている薬剤耐性菌が生まれるメカニズムの一つでもあります。プラスミドの中でも、接合伝達性プラスミドと呼ばれるグループのものは自身に備えた機構を用いて積極的な細胞間移動を行います。この時、プラスミドが移動可能な細菌の系統的な多様性を接合伝達の宿主域と呼び、限られた種にしか伝達できない狭宿主域プラスミドと、系統的に多様な細菌間を移動できる広宿主域プラスミドが存在しています。薬剤耐性伝播のプロセスを理解し対処する上で、多様な系統間で薬剤耐性遺伝子を伝播させられる広宿主域プラスミドの重要性は論を俟ちませんが、そもそも広宿主域が実現されるメカニズムや、広宿主域プラスミドと狭宿主域プラスミドとを区別し特徴づける因子が存在するのかも解明されておらず、この分野の大きな課題となっていました。
そこで本研究チームは、接合伝達が活発な腸内環境に生息し、肺炎桿菌(Klebsiella pneumoniae)など臨床的に重要な種を多く含む細菌群であるEnterobacterales(腸内細菌目)に注目し、公共データベースに登録されているこの系統群由来の接合伝達性プラスミドのDNA配列情報を網羅的に解析しました。その結果、広/狭宿主域プラスミドを特徴付ける遺伝子としてそれぞれhns、psiBを発見しました。プラスミドからの遺伝子発現を抑制することが知られているhnsと宿主のストレス応答を抑制するpsiBは対照的な機能を備えており、それぞれの宿主域に対応するプラスミドが異なった適応を遂げてきたことを示唆しています。これを裏付けるように、hns、psiBを保持するプラスミドの割合は、宿主域の拡大に対応してそれぞれ増加/減少し(図1a)、排他的な分布を示していました(図1b)。
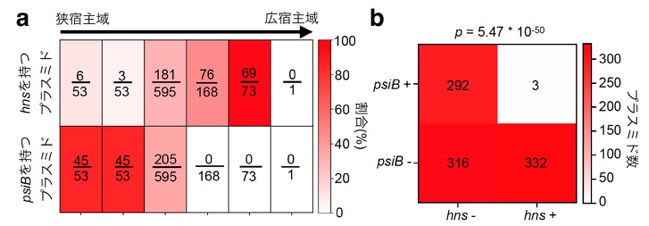
図1:(a) hnsを持つプラスミドの割合は宿主域が広いほど高く、psiBを持つプラスミドの割合はその逆の傾向を示した。各分数の分母と分子はそれぞれ各宿主域に属するプラスミドの総数とそのうちpsiB/hnsを保持しているものの数を表す。(b)psiBとhnsはプラスミド中に排他的に分布した。各数字はpsiB/hnsの有無により4パターンにプラスミドを分けた際の各パターンのカウントを表す。
各タイプのプラスミドの遺伝子セットやその他の配列的特徴は、それぞれが全く異なった適応を遂げたことを示唆していました。例えば、宿主のストレス応答を阻害するタンパク質であるpsiBを持つプラスミドは、宿主に存在する免疫系(注3) をはじめとするさまざまな機構を阻害することで自身を守る仕組みを備えており、転写抑制因子であるhnsを持つプラスミドが自身からの転写を抑制することで宿主に与える負荷を減らす点と対照的でした(図2)。これらの特徴は、進化生態学における生物の生存戦略になぞらえ、それぞれ「操作戦略」「ステルス戦略」と名付けられました。重要な点として、操作戦略は宿主の特定の機構を標的とするため、その標的を持つ宿主でしか機能しません。一方で、ステルス戦略はプラスミド自身を標的とするため、宿主を選ばずに普遍的に機能します。これらの戦略の「標的」の違いが、それぞれが狭宿主域と広宿主域に特徴的である理由の一つだと考えられます。
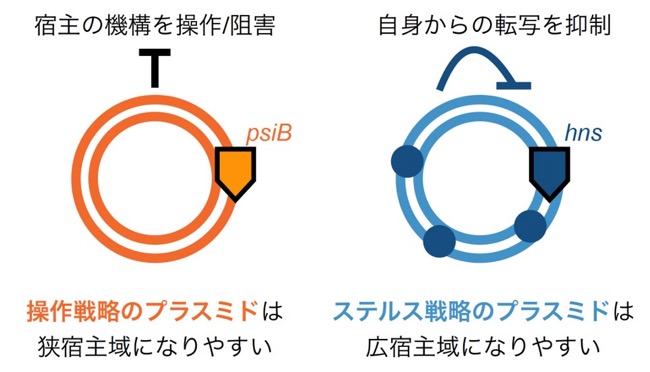
図2:psiBを持つプラスミド(オレンジ)と、hnsを持つプラスミド(水色)に特徴的な生存戦略。
さらなる解析の結果、操作戦略、ステルス戦略を持つプラスミドは、どちらも薬剤耐性遺伝子を特に多く保持することがわかりました。プラスミドのとる戦略の違いが、薬剤耐性遺伝子の伝播パターンに及ぼす影響を調べるために、2025年現在世界中で蔓延している48個の薬剤耐性遺伝子が、過去のどのタイミングで、どのタイプのプラスミド上から検出されてきたのかを示すデータセットを作成し解析しました。その結果、hnsを持つプラスミドは、psiBを持つプラスミドより早期に薬剤耐性遺伝子を獲得することがわかりました。この結果は、図3aに示されている例のように、薬剤耐性遺伝子は、①誕生したのち②まずhnsを持つステルス戦略のプラスミドに獲得され、その後で③psiBを持つ操作戦略のプラスミドなどにより拡散されるという、薬剤耐性遺伝子拡散の「ステルス・ファースト」モデルを提唱しました(図3b)。
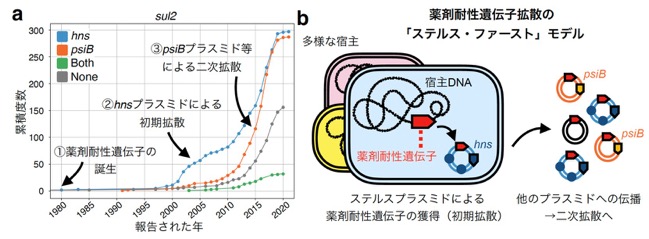
図3: (a) 2025年現在、世界中に蔓延している薬剤耐性遺伝子の一つであるsul2を保持しているプラスミドが検出されたタイミングをプラスミドの戦略タイプ別に示した。横軸は各プラスミドが検出された年を、縦軸は戦略タイプ別の検出回数の累積度数である。(b) この研究で提唱された「ステルス・ファースト」モデルの模式図。
この成果は、接合伝達性プラスミドの進化・生態をより深く理解するために、プラスミドの「生存戦略」という新たな枠組みを提唱するものです。どのようなプラスミドが広宿主域になりやすいのか、あるいは薬剤耐性遺伝子伝播の各段階がどのようなプラスミドにより担われているのか、といった疑問は、従来の枠組み(例えばMOBタイピング(注4) などのプラスミド分類法)では答えるのが困難でしたが、本研究で提唱したプラスミドの生存戦略という概念はその一助となることが期待できます。
また、DNA分子にすぎないプラスミドが、あたかも戦略を進化させてきたかのように見える基礎科学的な面白さのみならず、プラスミドにより媒介される薬剤耐性遺伝子拡散を、初期拡散とそれに次ぐ二次拡散に分けて捉え、かつ初期拡散を担うグループを同定できたことは、臨床への応用に大きな意味を持ちます。更に将来的には、耐性遺伝子毎の今後の伝播リスクを評価し、hnsを持つプラスミドを標的とする介入により初期拡散を食い止めるなど、薬剤耐性遺伝子の拡散防止に向けた新たなアプローチの構築に貢献することが期待されます。
発表者・研究者等情報
カリフォルニア大学バークレー校 比較生化学専攻Innovative Genomics Institute
小野 隆一 博士課程学生
研究当時:東京大学理学部生物情報科学科 学部学生
東京大学
大学院理学系研究科 生物普遍性研究機構
今野 直輝 客員共同研究員(兼 スタンフォード大学医学部 博士研究員)
研究当時:同研究科博士課程学生
古澤 力教授(兼 理化学研究所生命機能科学研究センター チームディレクター)
大学院新領域創成科学研究科
西村 祐貴 助教
論文情報
-
雑誌名 Nucleic Acids Research 論文タイトル Host range and antibiotic resistance dissemination are shaped by distinct survival strategies of conjugative plasmids 著者 Ryuichi Ono*,Naoki Konno*, Yuki Nishimura,Chikara Furusawa (*責任著者) DOI 10.1093/nar/gkaf1479
研究助成
本研究は科研費(課題番号: 22H04925)、JST(課題番号: GteX JPMJGX23B2)の支援により実施されました。用語解説
注1 接合伝達供与菌と受容菌が性線毛により連結することで引き起こされる、一方向性のDNA転移。↑
注2 接合伝達性プラスミド
細菌のゲノムとは独立して存在する環状DNAであるプラスミドのうち、接合伝達に必要な機構をすべて自前で備えており、細菌から細菌へと能動的に伝達できるものを特に指す。↑
注3 宿主に存在する免疫系
細菌が、自身の細胞内に侵入するファージや外来プラスミドなどの外来遺伝因子を排除・不活化するために備えている防御機構を指す。代表的なものとして、制限修飾系やCRISPR-Casシステムが挙げられる。↑
注4 MOBタイピング
接合伝達性プラスミドが備えているリラクセース(relaxase)遺伝子の配列を用いたプラスミドの分類法、あるいはそれにより割り当てられたグループ名のこと。この遺伝子は進化速度が比較的遅く、その配列の違いによっていくつかの明確なグループに大別される。そのため、接合伝達性プラスミドのグループ分けや、それらの系統関係を調べるために広く利用される。↑
 東京大学 研究
東京大学 研究