自然免疫応答を制御する一本鎖核酸分解メカニズムを解明
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | PLD3やPLD4の遺伝子多型に起因する神経変性疾患や炎症性疾患の新たな治療法の開発に貢献することが期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
掲載日:2025年12月19日
概要
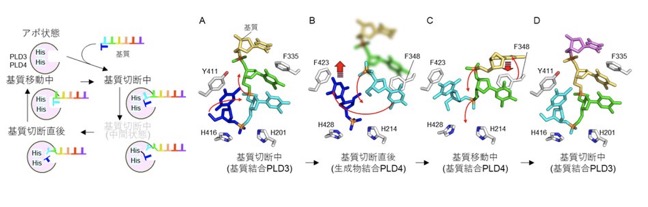
東京大学大学院薬学系研究科の平野良憲 助教、江﨑和貴子 大学院生(研究当時)、清水敏之 教授、同大学大学院新領域創成科学研究科の大戸梅治 教授、千葉大学未来粘膜ワクチン研究開発シナジー拠点の三宅健介 特任教授、佐藤亮太 特任助教らによる研究グループは、リソソームにおいて一本鎖核酸を分解するエキソヌクレアーゼPhospholipase D3(PLD3)、および PhospholipaseD4(PLD4)の基質が結合していないアポ構造、基質結合構造および基質切断直後の生成物結合構造をクライオ電子顕微鏡単粒子解析の手法で決定しました。異なる基質と結合した状態の構造解析から、PLD3は分解する基質に応じて基質結合ポケットを再構築することを発見しました。また、切断された核酸が結合ポケットから放出され、基質が再度切断される状態へ再編成される際に経る準安定状態を可視化することに成功し、PLD3およびPLD4が一本鎖核酸を末端から効率的に連続して分解する分子機構を明らかにしました。本研究成果はPLD3やPLD4の遺伝子多型に起因する神経変性疾患や炎症性疾患の新たな治療法の開発に貢献することが期待されます。リリース文書 (PDFファイル: 333KB)
論文情報
Yoshinori Hirano, Wakiko Ezaki, Ryota Sato, Umeharu Ohto, Kensuke Miyake, Toshiyuki Shimizu, "Mechanistic insights into single-stranded DNA degradation by lysosomal exonucleases PLD3 and PLD4 from structural snapshots,"Nature Communications: 2025年12月11日, doi:10.1038/s41467-025-66261-2.論文へのリンク (掲載誌
 )
)
科学と技術
このページの内容に関する問い合わせは薬学系研究科・薬学部までお願いします。
お問い合わせ
 東京大学 研究
東京大学 研究