がん細胞内の「現地」で光るポリマーを化学合成
がんの診断を改革する生体内合成化学技術
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | 生体内のがん特異的代謝環境を生かした初の細胞内ポリマー化法であり、生体内合成化学治療への第一歩として、診断・手術支援などへの応用が期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
手術支援/分子構造/固体NMR/アンモニア/クリック反応/ゲル化/環化付加反応/高分子/高分子合成/高分子反応/触媒反応/生細胞/保護基/有機合成化学/結合状態/アミン/ハイドロゲル/金属触媒/選択性/ベンゼン/エタノール/プラスチック/ポリマー/マイクロ/高分子材料/水素原子/熱分解/生体内/診断法/エチレン/アスコルビン酸/アルデヒド/生体組織/子宮/浸潤/ポリアミン/リンパ球/前立腺がん/がん化/グルタチオン/組織工学/不均一性/イミン/がん細胞/がん治療/ドキソルビシン/バイオイメージング/プロドラッグ/マウス/環化反応/血液/合成化学/細胞培養/迅速診断/代謝物/内分泌/付加反応/副作用/有機合成/誘導体/臨床試験/がん患者/化学療法/抗がん剤/脂質/手術/乳がん/臨床研究
2025年12月12日 公開
概要
東京科学大学(Science Tokyo) 物質理工学院 応用化学系の田中克典教授(理化学研究所(理研) 開拓研究所 田中生体機能合成化学研究室 主任研究員)、アンバラ・プラディプタ助教(理研客員研究員)、川口慎司大学院生(博士後期課程2年、理研研修生)、佐藤浩太郎教授らの共同研究グループは、がん細胞で過剰に産生される代謝物「アクロレイン[用語1]」を利用し、がん細胞内でのみポリマー[用語2a]を自発的に合成できる革新的なポリマー化技術の開発に成功しました。本研究成果は、乳がん患者から摘出された臨床サンプルにも適用できたことから、生体内のがん特異的代謝環境を生かした初の細胞内ポリマー化法であり、生体内合成化学治療への第一歩として、診断・手術支援などへの応用が期待されます。
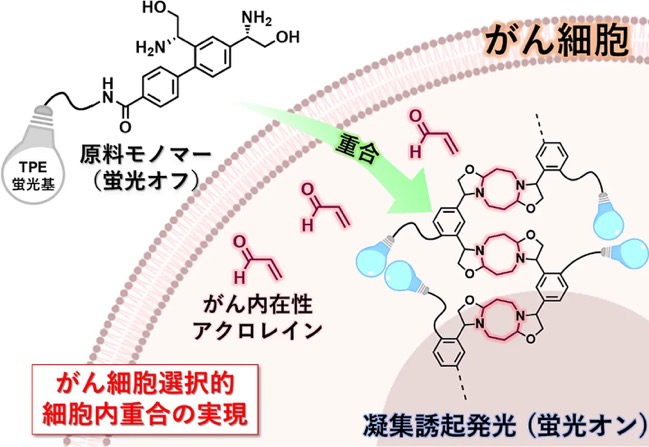
この手法では、設計された原料モノマー[用語2b](meta-フェニレン-ビス(2-アミノエタノール))が触媒や外部刺激を一切必要とせずに、がん細胞内部に存在するアクロレインと選択的に二量化カスケード反応[用語3]を起こして8員環(1,5-ジアザシクロオクタン環)を構築しながら高分子鎖を形成します。さらに、このモノマーに凝集誘起発光(AIE)[用語4]特性を有するテトラフェニルエチレン(TPE)蛍光基を組み込むことで、ポリマーが形成されると同時に蛍光がオンになる現象が起こり、がん細胞だけを選択的かつリアルタイムに可視化することが可能となりました。
本研究成果は、科学雑誌「Angewandte Chemie International Edition」の上位5%の重要論文(Very Important Paper:VIP)に選出され、12月4日付でオンライン掲載されました。
背景
生体関連化学分野において、高分子材料は薬物送達やバイオイメージング、生体組織工学などに広く応用されています。しかし、それらの高分子材料は「フラスコで合成してから細胞内に導入する」必要があり、膜透過性の低さや細胞内での安定性に課題がありました。田中教授らは、原料をあらかじめ細胞内に届けて、「細胞内現地でポリマーを合成し、その場で機能を発揮させる」ことを提案し、今回初めて実現させることができました。田中教授らはこれまでに、一級アルキルアミン(アンモニアの1個の水素原子をアルキル基で置換した化合物)類やアミノエタノール類とアクロレインが反応すると、二量化カスケード反応によって8員環(1,5-ジアザシクロオクタン環)を有する化合物を温和な条件で得られることを報告しています注1)。さらに、さまざまながん細胞でアクロレイン分子(図1赤色で示した化合物)が大量に産生されていることを見いだしました注2)。アクロレインは脂質過酸化やポリアミン代謝過程で生じ、がん細胞内でのアクロレイン生産量は通常の細胞内での生産量の10~100倍に達することが報告されています。
共同研究グループは、がん細胞内に豊富に存在するアクロレインの高分子構造に取り込まれるユニークな性質を利用して、アクロレインを用いたがん細胞の識別手法の開発を試みました。
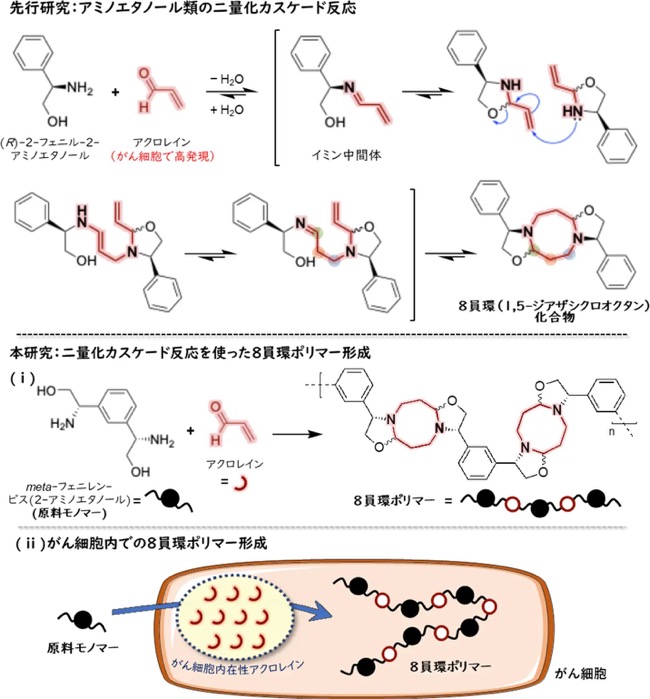
がん細胞だけに豊富に存在するアクロレインが、エタノールと反応して8員環を温和かつ迅速に形成することができる。本研究ではこの知見を応用し、がん細胞内のアクロレインを”起爆剤”として8員環ポリマーの合成に挑んだ。
注1)2016年3月15日理研プレスリリース「不安定な共役イミンが起こす多様な環化反応を発見」
注2)2018年11月28日理研プレスリリース「有機合成反応で乳がん手術を改革」
研究成果
本研究では、アミノエタノール類の構造を改良して、がん細胞で異常に多く産生される内在性代謝物「アクロレイン」を“起爆剤”として、がん細胞内でのみ8員環ポリマーが自発的に合成される革新的なポリマー化反応(図1下)を開発しました。この反応で得られる8員環ポリマーは、アクロレインが高分子の構造に取り込まれるユニークな高分子であり、アクロレインが少ない正常細胞ではこの反応は起こりません。さらに、この反応をフラスコからがん細胞、がん臨床レベルまで適用させて、がん患者の新しい診断技術を実現しました。具体的な研究手法は次の通りです。共同研究グループはまず、アクロレインと選択的に反応する二つのアミノエタノール構造を持つ原料モノマー(meta-フェニレン-ビス(2-アミノエタノール))を5工程の化学変換を経て合成しました。この原料モノマーを水中・室温下で試薬のアクロレインと反応させると、瞬時に8員環構造が連なったポリマーが得られました(図2a)。実際に熱重量分析[用語5]および固体NMR分析[用語6]の結果から、原料モノマーとアクロレインが二量化カスケード反応によって、8員環構造に連なっていることを確認しました(図2b)。この反応において、触媒や外部刺激は一切必要ありません。さらに、生体内に存在するグルタチオンやアスコルビン酸の存在下や、細胞培養液中でも重合が確認されたことから、重合は生体内でも進行する可能性を示しました(図2c)。
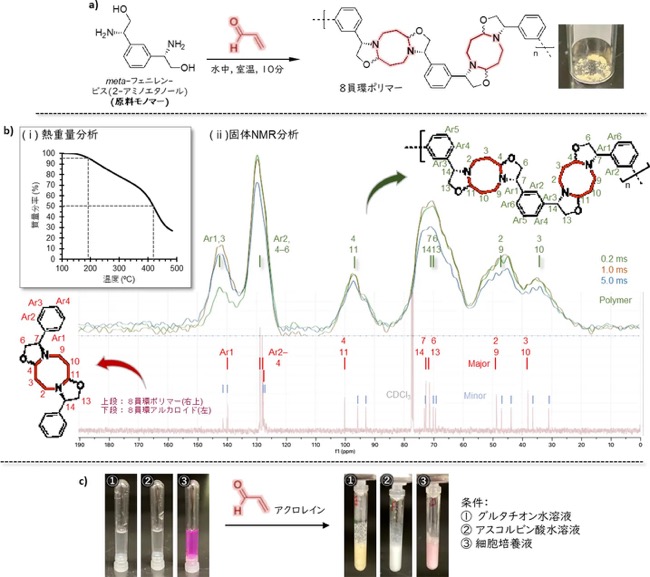
(a)meta-フェニレン-ビス(2-アミノエタノール)を水中でアクロレインと反応させると、瞬時に黄色のポリマー沈殿が生じる。
(b)熱重量分析や固体NMR分析の結果から、アミノエタノールとアクロレインが重合して8員環ポリマーを形成していることが実証された。
(c)水中だけでなく、生体内に普遍的に存在する(1)グルタチオンや(2)アスコルビン酸存在下、さらに(3)細胞培養液中でも黄色~白色の沈殿を形成したことから、生理的条件下でも重合が進行し、8員環ポリマーを形成できることを示した。
さらに共同研究グループは、テトラフェニルエチレン(TPE)蛍光基を組み込んだ原料モノマー「TPE-AE」を合成しました。TPE蛍光基は凝集誘起発光と呼ばれる性質を持ち、TPE分子同士が密集すると強い青色蛍光を発します。TPE-AE原料モノマーをがん細胞に投与すると、ポリマー化によってTPE蛍光基が密集し、がん細胞だけが蛍光を発する「光る高分子反応」が実現します。実際にヒト子宮頸(けい)がん細胞(HeLa S3)やヒト前立腺がん細胞(PC3)、ヒト乳がん細胞(MCF-7・T-47D)といった複数のがん細胞では、アクロレインが過剰に生産されているため、がん細胞内での8員環ポリマー形成が起こったことで強い蛍光が観察されましたが、アクロレインが少ない正常乳腺細胞(TIG-3)では8員環ポリマーは形成されないためほとんど発光せず、蛍光の有無だけでがん細胞を識別できました(図3)。
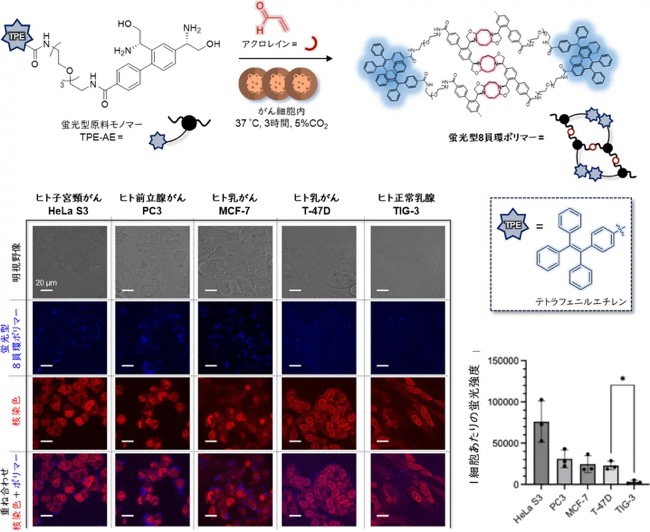
TPE-AEモノマーを4種のがん細胞および正常細胞に投与した結果、がん細胞に存在するアクロレインと原料モノマーが重合し、TPE蛍光基が密集したことで強い青色蛍光を観測できたのに対し、正常細胞では非常に弱い蛍光しか観測されなかった。
最後に、実際の乳がん患者から手術中に取り出されたがんおよび正常組織サンプルを用いてインプリントサイトロジー[用語7]実験を行いました。その結果、TPE-AE原料モノマーの溶液にそのサンプルを1分間浸すだけで、アクロレインが過剰に生産されているがん細胞では、8員環ポリマーの形成によって青色の蛍光を観察できました。一方で、アクロレインが少ない正常乳腺(TIG-3)組織では8員環ポリマーは形成されないためほとんど発光しませんでした(図4)。細胞レベルでの実験と同様に、蛍光の有無だけで、がん組織を迅速に識別できることを実証しました。
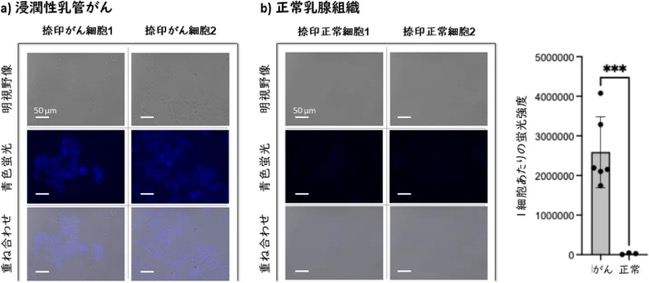
摘出直後の乳がん(浸潤性乳管がん)組織をTPE-AE原料モノマー溶液に1分間浸し、スライドガラスに捺印(なついん)して観察すると、がん組織由来の捺印細胞が明るく発光した。一方、正常乳腺組織は発光しなかった。蛍光強度の差でがんと正常細胞を判別できる可能性を示された。
今後の展開
今回の研究では、がん細胞内の代謝物として発生するアクロレインを有効利用して、試薬を入れるだけでがん選択的に光るポリマーを化学合成することに成功しました。特に、外部からの刺激や触媒を必要とせず、アクロレイン自体がポリマー構造に組み込まれることで選択性が生じる点が特徴です。この仕組みを活用して、がん患者の新しい診断技術を実現することができました。今後は、合成した8員環ポリマーに治療機能を持たせることで、診断と治療を融合した次世代のがん治療材料としての応用が期待されます。これにより、田中教授らが掲げる、がんの「生体内合成化学治療」の発展がさらに加速すると考えられます。
用語説明
- [用語1]
- アクロレイン:生体内で生成される反応性の高いアルデヒド化合物。田中生体機能合成化学研究室が、がん細胞内では普遍的に、外部から導入した試薬と有意に化学反応を起こすことができる高濃度(マイクロモーラー〜ミリモーラー程度(1マイクロモーラーは100万分の1モーラー、モーラーは1リットル当たりのモル数))でアクロレインが生成されることを発見した。
- [用語2a]
- ポリマー:モノマー(単量体)は「1個の分子単位」を意味する。今回の研究では、アミノエタノール類が該当し、アクロレインと反応して自ら連結する原料として働く。モノマーが鎖のように多数つながるとポリマー(高分子化合物)になる。プラスチックやタンパク質もポリマーの一種。今回の反応では、8員環構造が連なったポリマーを生成する。
- [用語2b]
- モノマー:用語2aを参照
- [用語3]
- 二量化カスケード反応:一級アルキルアミン類やアミノエタノール類がアクロレインと反応して生成されるイミン中間体が連鎖的な環化反応を経て8員環(1,5-ジアザシクロオクタン)骨格を形成する反応。開始剤や触媒なしに、水中・室温・短時間で反応が完結し、8員環化合物を定量的に得られる。2016年田中生体機能合成化学研究室が独自に開発した注1)。
- [用語4]
- 凝集誘起発光(AIE):蛍光分子や蛍光基が分散した状態では無蛍光だが、それらが物理的に凝集すると、その発光強度が強まる現象。テトラフェニルエチレンやその誘導体がAIE特性を持つことで知られている。AIE はAggregation Induced Emissionの略。
- [用語5]
- 熱重量分析:試料を加熱しながら重さの変化を測定することで、熱分解や揮発のしやすさを調べる手法。物質の熱的安定性を評価できる。
- [用語6]
- 固体NMR分析:固体試料中の原子の周囲環境を磁気的に観察し、構造や結合状態を調べる分析法。一般的な溶液NMRでは解析の難しい、難溶性の物質でも構造を解析できる。NMRはNuclear Magnetic Resonanceの略。
- [用語7]
- インプリントサイトロジー:手術直後の組織をスライドガラスに押し付け、短時間で細胞診を行う手法。特別な技術を必要とせず、迅速かつ簡単に行えるため、非常に有効な手段の一つである。
論文情報
- 掲載誌:
- Angewandte Chemie International Edition
- タイトル:
- Cancer-Selective Intracellular Polymerization via Acrolein-Driven Cyclodimerization Cascade
- 著者:
- Shinji Kawaguchi, Ambara R. Pradipta, Tomohiro Kubo, Akihiro Ishiwata, Takuma Sekiguchi, Hiromasa Yoshioka, Takaaki Hatano, Koji Morimoto, Tomonori Tanei, Kenzo Shimazu, Kotaro Satoh and Katsunori Tanaka
- DOI:
- 10.1002/anie.202518290
共同研究グループ
東京科学大学 物質理工学院 応用化学系教授 田中克典(理化学研究所 開拓研究所 田中生体機能合成化学研究室 主任研究員)
助教 アンバラ・プラディプタ(Ambara Pradipta)(理化学研究所 開拓研究所 田中生体機能合成化学研究室 客員研究員)
大学院生(博士後期課程2年)川口慎司(理化学研究所 開拓研究所 田中生体機能合成化学研究室 研修生)
教授 佐藤浩太郎
助教 久保智弘
大学院生(研究当時、修士課程)関口拓真
理化学研究所 開拓研究所 田中生体機能合成化学研究室
専任研究員 石渡明弘
基礎科学特別研究員 吉岡広大
大阪大学医学部附属病院 乳腺・内分泌外科
教授 島津研三
准教授 多根井智紀
大学院生 波多野高明
大阪国際大学 人間科学部 人間健康科学科
教授 盛本浩二

関連リンク
プレスリリース がん細胞内の「現地」で光るポリマーを化学合成—がんの診断を改革する生体内合成化学技術—(PDF)糖鎖とタンパク質の多価相互作用を解析する新規磁性リポソーム型バイオセンサを開発 | Science Tokyoニュース
クリック反応を使った自在な高分子合成手法の開発に成功 | Science Tokyoニュース
FTY720プロドラッグ(pro-FTY)がリンパ球減少を回避して乳がんの増殖を抑制することを明らかに | Science Tokyoニュース
副作用を劇的に抑えた抗がん剤ドキソルビシンの開発 | Science Tokyoニュース
臓器から臓器へと体内を自在に動く分子 | Science Tokyoニュース
マウス体内の血液で触媒を作り、がんに運んで化学治療 | 旧・東京工業大学
マウス体内でがんの糖鎖構造を合成化学的に変換 | 旧・東京工業大学
“生細胞での有機合成化学”による新しい乳がん術中迅速診断法(CTS法)の臨床試験を開始 | 旧・東京工業大学
がんに貼り付く極小サイズの分子接着剤 | 旧・東京工業大学
金触媒反応を引き金とするハイドロゲル化 | 旧・東京工業大学
極微量の触媒で抗がん剤を体内で大量生産 | 旧・東京工業大学
わずか窒素3原子でがんを見つけてα線治療 | 旧・東京工業大学
植物毒の「現地合成」でがん細胞の増殖阻害に成功 | 旧・東京工業大学
乳がん術中迅速診断多施設臨床研究を行う共同研究を開始 | 旧・東京工業大学
体内でベンゼン環を作る | 旧・東京工業大学
たった1回の投薬で効く体内触媒戦法 | 旧・東京工業大学
金属触媒で"変身"する保護基 | 旧・東京工業大学
世界初のマウス体内におけるタギング治療 | 旧・東京工業大学
体内での環化付加反応によるがん化学療法 | 旧・東京工業大学
がん細胞上で薬剤を化学合成 | 旧・東京工業大学
糖鎖の不均一性を秩序よく高次化してがんを見つける | 旧・東京工業大学
生体内の金属触媒反応で薬効と物性を制御する | 旧・東京工業大学
田中克典教授がアステラス病態代謝研究会の「2022年度最優秀理事長賞」を受賞 | 旧・東京工業大学
田中克典教授が日本化学会第37回学術賞を受賞 | 旧・東京工業大学
田中 克典 Katsunori Tanaka | Science Tokyo研究情報データベース(理工学系)
Ambara Rachmat Pradipta | Science Tokyo研究情報データベース(理工学系)
佐藤 浩太郎 Kotaro Satoh | Science Tokyo研究情報データベース(理工学系)
久保 智弘 Tomohiro Kubo | Science Tokyo研究情報データベース(理工学系)
田中克典研究室
田中克典研究室 | 物質理工学院 研究室検索サイト
佐藤浩太郎研究室
佐藤浩太郎研究室 | 物質理工学院 研究室検索サイト
物質理工学院 応用化学系
物質理工学院
理化学研究所
問い合わせ先
東京科学大学 物質理工学院 応用化学系教授 田中 克典
取材申し込み
理化学研究所 広報室 報道担当- Tel
- 050-3495-0247
- ex-press@ml.riken.jp
東京科学大学 総務企画部 広報課
- Tel
- 03-5734-2975
- Fax
- 03-5734-3661
- media@adm.isct.ac.jp
 東京科学大学 研究
東京科学大学 研究