世界初の紫外光応答イオンチャネルを発見
―光遺伝学への応用に期待―
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | 神経ネットワーク研究において有用な光遺伝学などで、紫外光に応答する特性を活かした分子ツールとしての応用が期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
アンテナ/インターフェース/データ駆動/インテリジェンス/人工知能(AI)/光エネルギー/海洋/強磁場/時間分解/超強磁場/分光学/スペクトル/磁場/太陽/レチナール/吸収スペクトル/光応答性/光化学/アーキア/光応答/光受容/光受容タンパク質/光受容体/青色光/太陽光/ラマン/光電流/可視光/光吸収/選択性/光照射/構造モデル/紫外線/イオン輸送/カリウム/センサー/ナノメートル/マルチスケール/光センサー/人工細胞/オプトジェネティクス/古細菌/哺乳類/リン酸/海洋細菌/植物ホルモン/タンパク質工学/共生細菌/原生生物/褐虫藻/微生物/チャネルロドプシン/ビタミン/ゲノム情報/細胞膜/脳神経科学/アデノシン/ラマン分光/酵素反応/神経ネットワーク/ホルモン/生理機能/光遺伝学/光操作/ATP/アミノ酸/イオンチャネル/カチオン/トランスクリプトーム/ビタミンA/ロドプシン/再生医療/細胞核/受容体/神経科学
研究成果
東京大学
発表のポイント
原生生物のアプソモナド類から、新種の光応答性イオンチャネルである「アプソモナドロドプシン」を発見しました。アプソモナドロドプシンは紫外光に応答して、細胞膜を乗り越えて陰イオンを輸送するこれまでにない機能を有しています。
今後は、神経ネットワーク研究において有用な光遺伝学などで、紫外光に応答する特性を活かした分子ツールとしての応用が期待されます。
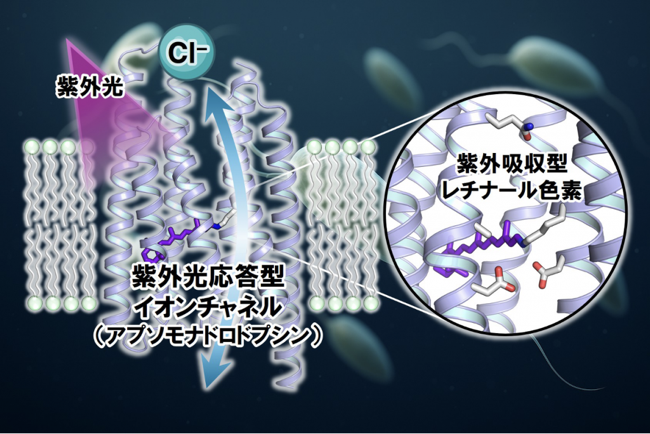
紫外光に応答して、イオンを輸送するアプソモナド類のロドプシン
発表概要
東京大学物性研究所の寳本俊輝特任研究員(研究当時)、永田崇助教、髙橋大翔大学院生、井上圭一准教授らによる研究グループは、原生生物(注1)の一種であり、動物や菌類に近縁で、真核生物(注2)の進化の理解に重要とされるアプソモナド類から、紫外光に応答する新しいタイプのイオンチャネルタンパク質である「アプソモナドロドプシン」を発見しました。本研究では、最近報告されたアプソモナド類のゲノム情報に着目し、光応答型の膜タンパク質である微生物ロドプシン(注3)に分類されるタンパク質を10種以上発見し、アプソモナドロドプシンと名付けました。そして、培養細胞を用いてタンパク質を発現し、分光学的および電気生理学的な実験手法によって研究を行うことで、これらアプソモナドロドプシンは光に応答してイオンを輸送する光開閉式のイオンチャネルであることが示されました。さらにそのうちのいくつかはエネルギーが高く波長の短い光である紫外線に応答する初めてのイオンチャネルであることが明らかとなりました。これらアプソモナドロドプシンは今後新たな生体分子ツールとして、神経研究に重要な光遺伝学などへの応用が期待されます。 全文PDF
発表内容
微生物ロドプシンは、ビタミンAの類縁体であるレチナール色素(注4)を使って太陽光を捉え、そのエネルギーを使って様々な機能を示す膜タンパク質のファミリーです。中でも、水素イオン(H+)を細胞外側に輸送し、細胞のエネルギー通貨であるアデノシン三リン酸(ATP)の合成などを駆動する、H+ポンプ型や、様々なイオンを濃度や電気的な勾配に沿って大量に輸送するイオンチャネル型の微生物ロドプシンが数多く調べられてきました。一方、近年ではこれらイオン輸送型は動物の脳などの神経細胞に発現させ、光で神経の活動を制御する光遺伝学(オプトジェネティクス)と呼ばれる技術が、神経科学分野や、視覚再生医療、神経疾患医療の分野などで大きな注目を集めています。しかし、微生物ロドプシンは約100ナノメートル(注5)の幅広い範囲の光に応答することから、異なる波長の光を用いて複数のロドプシンを駆動し、それによって複雑な細胞活動の光操作を達成するのは困難でした。この目的のため可視光領域(400–700ナノメートル)以外の波長に応答するロドプシンが必要とされていますが、そういった分子はこれまで知られていませんでした。
この様な状況の中、本研究グループはグラナダ大学(スペイン)や、イスラエル工科大学(イスラエル)との国際共同研究により、原生動物のひとつである、アプソモナド類に着目しました。これまでアプソモナド類は、動物や菌類に近縁で、真核生物の進化の理解に重要な生物種として知られていましたが、これらが持つタンパク質についてはあまり研究が行われていませんでした。そして、本研究グループがアプソモナド類のゲノム情報を調べたところ、10個以上の微生物ロドプシンが新たに見出され、アプソモナドロドプシンとして名付けられました。さらに、アプソモナドロドプシンでは、タンパク質の性質を決めるアミノ酸の配列が他の微生物型ロドプシンと大きく異なっており、これまでにない機能や物性を持つことが期待されました。
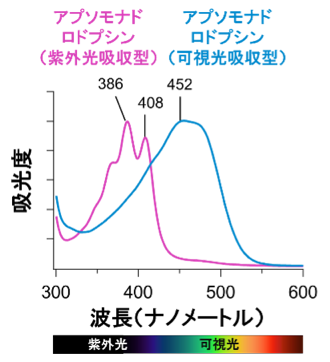
図1:紫外光吸収型(紫)と可視光吸収型(青)のアプソモナドロドプシンの吸収スペクトル
そこで本研究グループは、これらアプソモナドロドプシンの情報をコードしたDNAを新たに合成し、それを用いてアプソモナドロドプシンのタンパク質を実験室内において、培養された哺乳類の細胞内に発現させました。その結果、半分以上のアプソモナドロドプシンにおいて、タンパク質に結合したレチナール色素の吸収波長が可視光領域ではなく、より短波長の紫外光領域にあることが明らかとなりました(図1)。さらに、電気生理学的計測から、細胞膜上にあるアプソモナドロドプシンに紫外光が照射されると、分子の中を陰イオンが流れることを示す光電流信号が観測されました(図2)。この結果から、アプソモナドロドプシンは紫外光に応答して陰イオンを輸送する初めてのタイプのイオンチャネルであることが明らかとなりました。
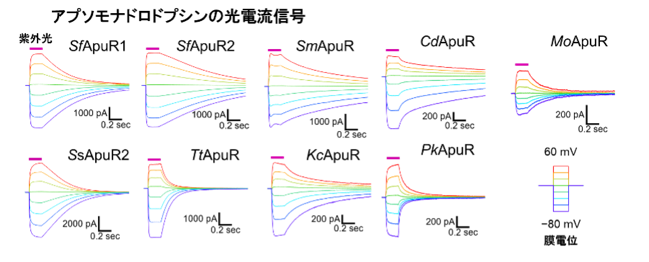
図2:紫外光照射に伴って駆動される、アプソモナドロドプシンのイオン輸送を表す光電流信号
加えて、本研究グループはアプソモナドロドプシンだけが、紫外光に応答できる謎を解明するため、分子の構造を生化学的に調べました。その結果、可視光を吸収するアプソモナドロドプシンでは、通常の微生物ロドプシンと同様にレチナール色素の根元にH+が結合しているのに対し、紫外吸収型のアプソモナドロドプシンではそのH+が解離することでレチナール色素の吸収波長が紫外光の領域まで短波長シフトしていることが明らかとなりました(図3)。またアミノ酸改変タンパク質を用いた実験により、このレチナール色素へのH+の結合とそれに伴う応答波長の変化が、色素周辺のわずかなアミノ酸残基によって制御されていることも示されました。
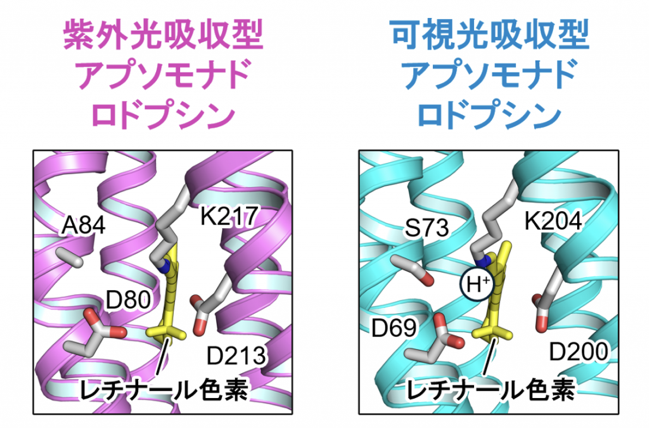
図3:紫外光吸収型(左)と可視光吸収型(右)アプソモナドロドプシンの構造モデル。
可視光吸収型のレチナール色素に結合している水素イオン(H+)が紫外吸収型のアプソモナドロドプシンでは解離することによって、レチナールの吸収が紫外光の領域にシフトすると考えられる
今後の展望
今回の研究により、アプソモナド類が独自の光化学的性質を持つアプソモナドロドプシンを用いて、光を感知していることが示されました。先行研究の中で、アプソモナド類は青色光など、エネルギーが高く細胞のDNAなどにダメージを与える短波長の光に対して忌避反応をしめすことが報告されていることから、そのための光センサーの機能をアプソモナドロドプシンが担っている可能性がありますが、今後新たな研究によりその問題が解明されると期待されます。
一方で、アプソモナドロドプシンは従来のイオン輸送型の微生物ロドプシンと比べて、大きく短波長の光に応答できることから(図4)、他の分子と組み合わせることで、複数の波長の光による複雑な細胞活動の操作を可能にする新たな分子ツールとして、光遺伝学分野などでの利用が期待されます。
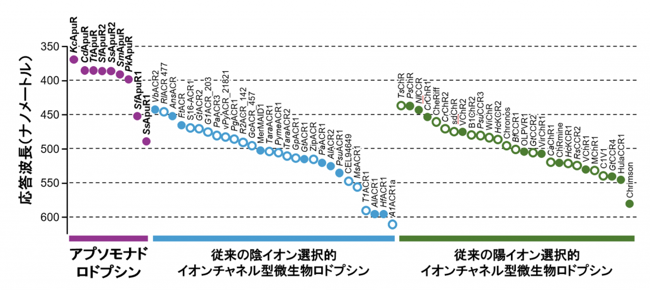
図4:アプソモナドロドプシンと従来のイオンチャネル型微生物ロドプシンの応答波長の比較
発表者・研究者等情報
東京大学物性研究所
井上 圭一 准教授
永田 崇助教
寳本 俊輝 特任研究員(研究当時、現:国際高等研究所ニューロインテリジェンス国際研究機構 特任研究員)
大学院新領域創成科学研究科
髙橋 大翔 修士課程
論文情報
雑誌名:Proceedings of the National Academy of Sciences of the United States of America (PNAS)題 名:Apusomonad rhodopsins, a new family of ultraviolet to blue light absorbing rhodopsin channels
著者名:Luis Javier Galindo†,*, Shunki Takaramoto†, Takashi Nagata†, Andrey Rozenberg†, Hiroto Takahashi, Oded Béjà, Keiichi Inoue* †(共同)筆頭著者、*責任著者
DOI:10.1073/pnas.2510619122
研究助成
本研究は、日本学術振興会(JSPS) 科学研究費助成事業(学術変革領域研究(A)「分子サイバネティクス―化学の力によるミニマル人工脳の構築」における「微生物ロドプシンを用いた光による人工細胞への高速刺激入力法の開発」(研究代表者:井上 圭一、課題番号:JP23H04404)、学術変革領域研究(A)「1000テスラ超強磁場による化学的カタストロフィー :非摂動磁場による化学結合の科学」における「1000 T化学反応の探索と解明」(研究分担者:永田 崇、課題番号:23H04863))、および科学技術振興機構(JST) 戦略的創造研究推進事業(CREST「データ駆動・AI駆動を中心としたデジタルトランスフォーメーションによる生命科学研究の革新(研究総括:岡田 康志)」における「AIが先導するオートメーションタンパク質工学の創出」(研究代表者:井上 圭一、課題番号:JPMJCR22N2)」)、日本医療研究開発機構(AMED)脳神経科学統合プログラム「紫外光を用いた光遺伝学の創生」(研究分担者:寳本俊輝 、永田 崇、課題番号: JP24wm0625115)、文部科学省・学際領域展開ハブ形成プログラム・マルチスケール量子-古典インターフェース研究コンソーシアム(課題番号:JPMXP1323015482による支援を受けて行われました。用語解説
- (注1)原生生物
- 細胞内に細胞核を持つ生物種の総称。生物全体は細菌、古細菌(アーキア)、真核生物の三つに分類され、遺伝学研究により、真核生物は20億年ほど前に、ヘイムダル古細菌が属するプロメテ古細菌に近縁な古細菌の一部から進化したと考えられています。
- (注2)真核生物
- 細胞内に細胞核を持つ生物種の総称。生物全体は細菌、古細菌(アーキア)、真核生物の三つに分類され、遺伝学研究により、真核生物は20億年ほど前に、古細菌の一部から進化したと考えられています。
- (注3)微生物ロドプシン
- 7回膜貫通型の光受容タンパク質であり、ビタミンAの類縁体であるレチナール色素と結合しています。これら微生物ロドプシンはレチナール色素を用いて太陽光を捉え、その光エネルギーを使って主に細胞内外への水素イオンを含むさまざまなイオンの輸送を行います。そして、微生物ロドプシンは細菌、古細菌(アーキア)、真核微生物のほか、巨大ウイルスにまで広く分布することが知られています。
- (注4)レチナール色素
- 通常アミノ酸は可視領域に吸収を持たないため、アミノ酸で構成されるタンパク質もそれ単体では可視光を利用することができません。それに対してロドプシンはタンパク質内部に、体内の酵素反応でビタミンAから生じるレチナール色素と呼ばれる色素を結合しています。ロドプシンのタンパク質内部にあるレチナール色素が可視光を吸収するとその折れ曲がり構造が変化し、それを通じてタンパク質部分にも変化が起こり、さまざまな生理機能を発現することが可能になります。
- (注5)ナノメートル
- 1ナノメートル(1 nm)は、10億分の1メートルに対応しています。光の波長の単位にも使われています。
関連ページ
東京大学物性研究所 井上研究室2025.09.04プレスリリース海洋細菌の新たな光エネルギー獲得戦略 ―ロドプシンの集光アンテナと光サイクル加速色素の発見―
2025.06.23物性研ニュース褐虫藻の光受容体ロドプシンの独特な光化学的性質のしくみ — 構成的アプローチにより、その構造的要因を明らかに—
2025.05.29プレスリリースプロメテ古細菌から高感度な光駆動水素イオンポンプを発見 ―真核生物の出現に関わる古細菌による新たな光利用―
2025.03.21物性研ニュース植物共生細菌の光受容型水素イオンポンプタンパク質が、植物ホルモンにより活性化されることを発見
2024.10.30物性研ニュース環境メタトランスクリプトーム解析により、新奇な性質を持つ光駆動型カチオンチャネルを発見
2023.09.01プレスリリース微生物が光に反応してカリウムイオンを運ぶ しくみの解明と神経科学への応用 ―四半世紀ぶりに発見された全く新規のカリウムイオン選択性のしくみー
2023.05.16物性研ニュース光遺伝学の中心的なツール、チャネルロドプシンのチャネル開閉メカニズムを新開発時間分解ラマン分光系で解明!
2023.03.02 プレスリリース地球全体に分布するロドプシン保有細菌の新たな光エネルギー獲得戦略 ―キサントフィルを用いた集光アンテナの発見―
2022.06.17プレスリリース世界初 「光で駆動する巨大イオンチャネルタンパク質」を藻類から発見 ―深部脳領域の新たな診断・治療法の開発への応用に期待―
2022.02.03プレスリリース新規光駆動型イオンチャネルの構造解明と高性能分子ツールの創出 ~神経科学に光を当てる~
2021.03.30プレスリリースアスガルドアーキアの持つ、光エネルギーを使って 水素イオンを取込むタンパク質の構造を解明
2020.04.11プレスリリース真核生物の祖先に最も近縁なアスガルド古細菌の持つ、 新しい光受容タンパク質の機能を解明
(公開日: 2025年10月15日)
 東京大学 研究
東京大学 研究