老化で神経細胞は“落ち着き”を失う?
――遺伝子発現の“土台”の変化が脳の機能低下につながる可能性――
【注目の成果:共同研究・産学連携のためのチェックポイント】
 | 加齢性によりリスクが向上する神経疾患の発症メカニズムの解明につながることが期待 |
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
高齢化社会/神経系/ヒストン/ダイナミクス/神経発達/脳発達/分子神経生物学/クロマチン構造/免疫系/クロマチン/ニューロン/短期記憶/RNA/マウス/神経回路/神経細胞/神経生物学/神経変性/創薬/転写因子/脳機能/ゲノム/遺伝子/遺伝子発現/加齢/海馬/高齢化/神経疾患/生活の質/認知機能/老化
2025年10月2日
/ 最終更新日時 :2025年10月2日
adiqb
分子神経生物学研究分野
発表のポイント
◆マウス海馬の老化に伴う遺伝子発現とエピゲノムの変化をシングルセルレベルで解析しました。◆老化に伴ってニューロンにおける脳発達や応答性に関わる遺伝子がエピゲノムレベルで活性化していることを発見しました。
◆加齢性によりリスクが向上する神経疾患の発症メカニズムの解明につながることが期待されます。

老化したニューロンのクロマチン(右側)は若いとき(左側)よりオープンになる(開花する)
発表概要
東京大学定量生命科学研究所のMerve Bilgic(メルべ ビルギーチ)助教と岸雄介准教授による研究グループは、マウスの脳の老化における遺伝子の働きの変化を細胞1つ1つで詳しく解析し、神経細胞(ニューロン)(注1)の老化メカニズムの一端を明らかにしました。超高齢化社会の現代では、脳の老化に伴う認知機能の低下が大きな社会問題になっています。本研究では、若いマウスと高齢のマウスの脳から、記憶などをつかさどる海馬(注2)という領域を採取しました。そして最新技術を用いて、1つの細胞の中から「遺伝子の働きの結果」と「遺伝子の働きやすさ(エピゲノム状態)」(注3)を同時に計測しました。その結果、脳の情報伝達を担うニューロンは、老化とともに、本来は脳が発達する時期や刺激応答時に働く遺伝子などが働きやすい状態になっていることを発見しました。
これは、神経細胞が外部からの刺激に過剰に反応しやすくなる原因になると考えられ、適切な神経回路の維持を妨げる可能性があります。この成果は、脳が老化する根本的な原理の解明や、将来の加齢性神経疾患の理解に貢献することが期待されます。
発表内容
超高齢化社会を迎えた現代において、脳の老化は誰もが向き合う重要な課題です。認知機能や記憶力が衰えることは、私たちの生活の質(QOL)に直結します。脳の老化や、それに伴う病気を防ぐことは、現代社会で暮らす全ての人にとって大きな関心事になっています。脳の機能が低下する主な原因は、脳内で情報伝達を担う「ニューロン(神経細胞)」の働きの異常にあると考えられています。しかし、脳はニューロンだけでなく、それを支える多様な細胞の集合体です。そのため、老化によってどの細胞にどのような変化が起きているのかを詳しく調べることは重要な課題でした。
そこで本研究では、生物の「設計図」である遺伝子がどれだけ「実際に使われているか」がわかる遺伝子発現と、その「使われやすさの土台」であるエピゲノム状態を、細胞1つ1つで“同時に”調べることができるシングルセルマルチオーム解析(注4)という最新技術を用いました。老化の影響を受けやすい脳の海馬という領域を、若いマウスと高齢マウスから採取して解析した結果、多種多様な細胞の種類を特定し、それぞれの細胞で老化による変化を分離して分析することに成功しました(図1)。
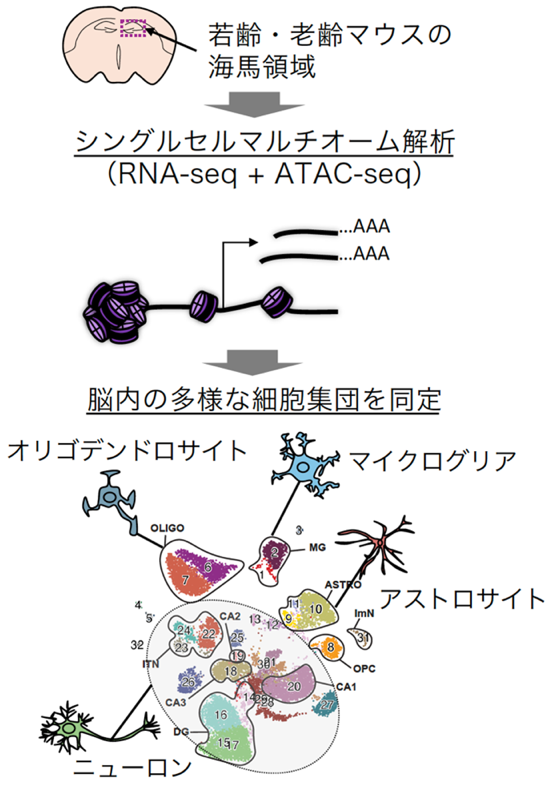
図1. シングルセルマルチオーム解析によって若齢・老齢マウス海馬の多様な細胞集団を同定した
細胞の種類ごとに詳しく比較すると、特にニューロンにおいて、遺伝子の実際の働き以上に、その「働きやすさの土台」であるエピゲノムが大きく変化していることが明らかになりました。遺伝子を、体の設計図がすべて書かれた「百科事典」に例えるなら、エピゲノムはどのページを読むべきかを示す「付箋」のような役割をしています。私たちの研究で、老化によってこの付箋が間違ったページに貼られてしまい、本来は読めないように閉じておくべき神経発達や刺激応答に関わる遺伝子などが、いつでも開けて読める準備ができてしまっている状態になっていることが分かりました。
さらに、このエピゲノムの変化を引き起こす原因を探るため、高齢ニューロンで働きやすくなっている遺伝子の周辺を詳しく調べました。その結果、Bach2(注5)というタンパク質が結合する目印が数多く見つかりました。このBach2は、AP-1と呼ばれる転写活性化因子と拮抗して、遺伝子の働きを抑える「ブレーキ」のような役割を持つと考えられます。実際に、Bach2は若いニューロンに多く、高齢ニューロンでは減少していました。この「ブレーキ役」が減少することが、遺伝子が過剰に働きやすい状態を生み出す一因である可能性が考えられます(図2)。
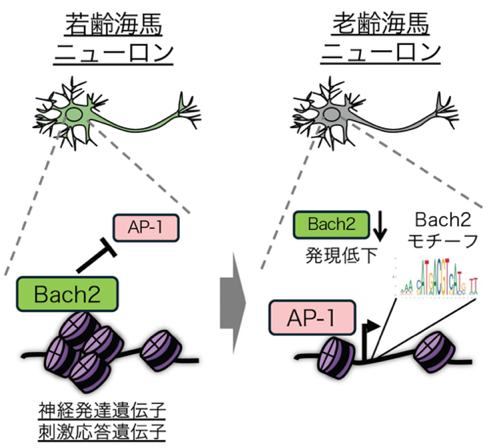
図2. ニューロンの老化に伴って神経発達・刺激応答遺伝子のエピゲノム状態が活性化した
今回の研究により、ニューロンは老化によって、脳の発達や刺激への応答に関わる遺伝子が過剰に働きやすい「落ち着きのない状態」になっていることが示唆されました。これは、神経細胞が些細な刺激に過敏になったり、必要な時にうまく働けなくなったりすることにつながり、神経変性や認知機能の低下の基盤となっている可能性があります。本研究の成果は、脳の老化の原理をさらに深く解き明かし、将来の加齢性神経疾患の予防や治療法の開発につながるものと期待されます。
関連情報
「プレスリリース①ニューロンの核は老化するとシワシワになり、かたくなる」(2023/7/25)
ニューロンの核は老化するとシワシワになり、かたくなる ――脳の加齢に伴ってニューロン核のダイナミクスが低下する――
発表者・研究者等情報
東京大学定量生命科学研究所
岸 雄介 准教授
Merve Bilgic 助教(メルべ ビルギーチ)
研究助成
本研究は、科研費「先進ゲノム支援(課題番号:16H06279)」、「新学術領域研究(課題番号:22H04687)」、「学術変革領域研究(A)(課題番号:23H04214)」、「学術変革領域研究(A)(課題番号:24H01227)」、「基盤研究(B)(課題番号:24K02020)」、AMED-PRIME、武田科学振興財団、上原記念生命科学財団、旭硝子財団、中外創薬科学財団、アステラス病態代謝研究会、小野薬品がん・免疫・神経研究財団、日立財団の支援により実施されました。用語解説
(注1)ニューロン神経系を構成する細胞で、電気信号や化学信号によって情報を伝達する役割を持つ。ほとんどのニューロンは発生期に産生され、一生入れ替わることなく脳内で働き続ける。
(注2)海馬
様々な脳機能に関わり、特に短期記憶という最近の出来事を記憶するために重要な領域である。歳をとると最近のことを忘れやすくなるのは海馬の機能異常であると考えられている。
(注3)エピゲノム
遺伝子の配列自体は変えずに、遺伝子の働きを後天的にオン・オフする仕組みのこと。DNAやヒストンタンパク質の修飾、クロマチン構造のオープン具合などでオン・オフを制御する。
(注4)シングルセルマルチオーム解析
1つの細胞から遺伝子発現をRNA-seqにて、エピゲノム状態をATAC-seqにて同時に計測する手法。それぞれの細胞種ごとの情報を得ることができる。
(注5)Bach2
DNA配列を読み取って遺伝子の発現を制御する転写因子の一つ。神経系での働きは詳しく調べられていないが、免疫系では遺伝子の発現を抑制することが知られている。
アイキャッチ画像

雑誌名等
雑誌名:Aging Cell題 名:Age–associated transcriptomic and epigenetic alterations in mouse hippocampus
著者名:Merve Bilgic, Rinka Obata, Vlada-Iuliana Panfil, Ziying Zhu, Mai Saeki, Yukiko Gotoh, Yusuke Kishi*
DOI:10.1111/acel.70233
URL: https://onlinelibrary.wiley.com/doi/10.1111/acel.70233
問い合わせ先
東京大学定量生命科学研究所 先端定量生命科学研究部門 分子神経生物学研究分野准教授 岸 雄介(きし ゆうすけ)
Tel:03-5841-7827 E-mail:[email protected]
東京大学定量生命科学研究所 総務チーム
Tel:03-5841-7813 E-mail:[email protected]
 東京大学 研究
東京大学 研究