自然界最強の毒素の一つパリトキシンの作用機構を解明
―― パリトキシンはどのようにしてナトリウム・カリウムポンプを 陽イオンチャネルに変えるか ――
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
食物連鎖/閉じ込め/有機合成化学/カルシウムポンプ/選択性/高温環境/原子構造/カリウム/電子顕微鏡/電子顕微鏡法/ATPアーゼ/ウシ/酵素活性/テトロドトキシン/フグ/渦鞭毛藻/クライオ電子顕微鏡/ナトリウム/細胞膜/アデノシン/筋肉/ATP/アミノ酸/イオンチャネル/カルシウム/ステロイド/構造生物学/構造変化/合成化学/生体膜/有機合成/立体構造
2025年9月17日
/ 最終更新日時 :2025年9月17日
adiqb
膜蛋白質解析研究分野
東京大学定量生命科学研究所
発表のポイント
◆パリトキシンはアオブダイやハコフグ、ソウシハギ等の食中毒の原因となる海産毒物で生物界最強の毒物の一つであり、神経興奮の基盤を作るナトリウム・カリウムポンプを陽イオンなら何でも通すチャネルに変えてしまう。その機構をクライオ電子顕微鏡を用いて解明した。◆イオンを運ぶ蛋白質という意味で混同されることの多い「チャネル」と「ポンプ」の本質的違いも明らかになった。
◆毎年のようにパリトキシン様毒による食中毒が報告されているが、解毒剤開発への道を拓くものである。
発表概要
東京大学・豊島 近 特別教授(同大学定量生命科学研究所特任教授)と同研究所 金井隆太特任講師らによる研究グループは、パリトキシン(注1)がナトリウム・カリウムポンプ(注2)をどのようにして陽イオンであればほぼ何でも通すイオンチャネルに変えてしまうかを、同研究所に設置された最新鋭のクライオ電子顕微鏡を用い、世界で初めて明らかにしました。パリトキシンは生物界で最も強力な毒物の一つであり、ナトリウム・カリウムポンプがその標的蛋白質です。ポンプとチャネルの違い或いは類似性を明らかにするものとして、長らく待たれていた構造生物学研究です。この研究成果は今後パリトキシン中毒の解毒剤開発にも役立つことが期待されます。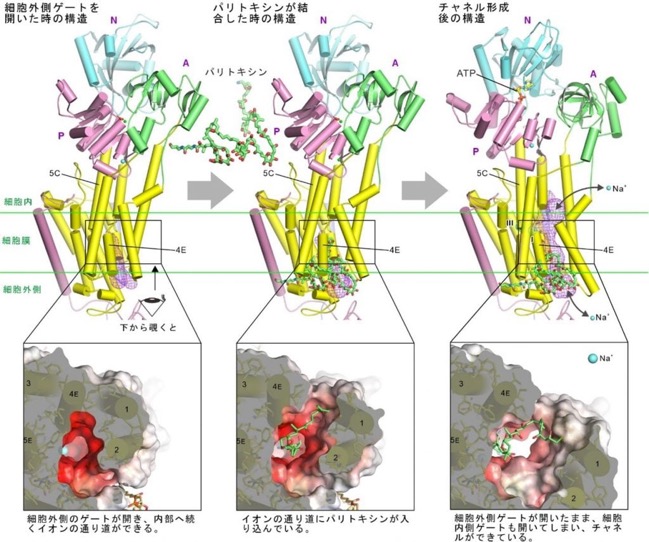
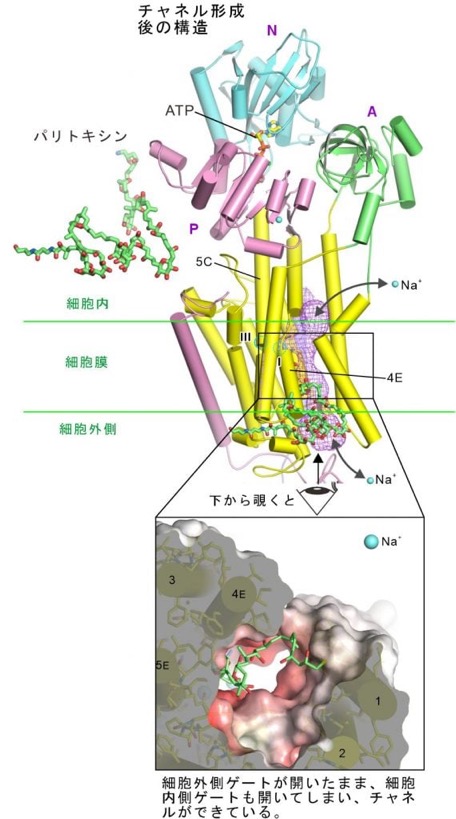
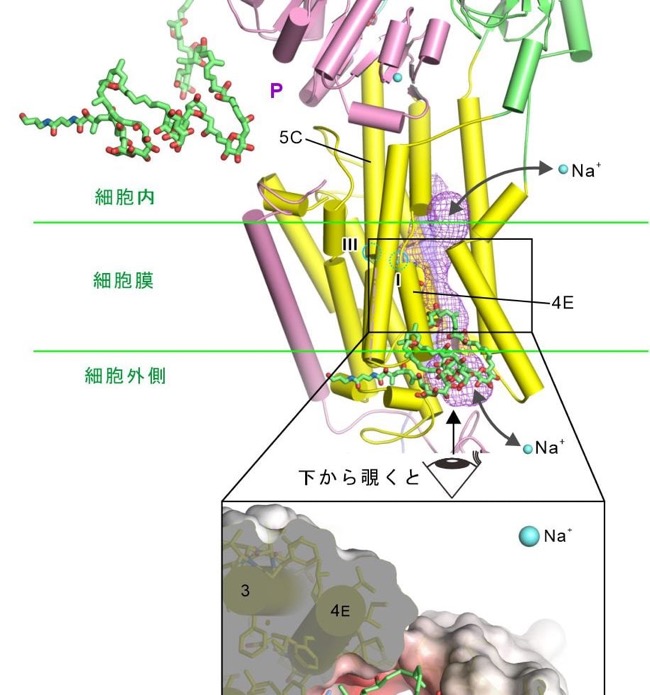
図1:ナトリウムカリウムポンプにパリトキシンが結合しチャネル化する様子
クライオ電子顕微鏡によって決定した三つの立体構造。紫の網は水が入れる空間を示す。
発表内容
1.ポンプとチャネルパリトキシンの標的がナトリウム・カリウムポンプ(Na+,K+-ATPase、以下NKAと略します)であることは古くから知られていました。ナトリウム・カリウムポンプは細胞膜を隔ててNa+(細胞外が濃い)とK+(細胞内が濃い)の濃度勾配を生み出す生体膜に存在する蛋白質(膜蛋白質)です。ミクロの手押しポンプのような動きをして、細胞内から外へとNa+だけを厳密に選択して高速で運搬します。また逆方向にK+を運搬します。Na+に限らず、物質は濃度の濃いところから薄いところへと流れるのが自然な流れですが、ポンプは薄いところから濃いところへと運ぶことができます。それをどのようにするかというと、図2のように、イオンの通り道には細胞内側と外側にゲートがそれぞれあるとします。まずは細胞内側のゲートを開けて、Na+がポンプ蛋白質に結合できるようにします。ポンプ蛋白質は細胞内側からはNa+しか結合できないようにデザインされています。Na+が結合したら細胞内側ゲートを閉じます。この状態ではNa+は蛋白質の中に閉じ込められたことになります。次に、細胞外側ゲートを開けて、結合していたNa+を押し出します。押し出されたら代わりにK+が結合できるようにします。K+が結合したら細胞外側ゲートを閉め、K+を蛋白質内に閉じ込めます。次に、細胞内側ゲートを開けてK+を追い出します。そうするとNa+がまた結合できるようになります。これを繰り返すわけです。ミソは二つあるゲートが順番に開閉し、同時には開かないということです。
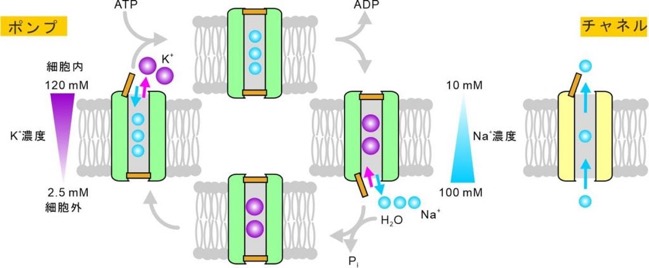
図2:イオンポンプとチャネルの概念的モデル
細胞内外でイオンの濃度には差がある。濃い方から薄い方へイオンを通すのがチャネルであり、濃度差に逆らって運搬するのがポンプである。チャネルのゲートは一つでよいが、ポンプには二つ必要で、同時に開いてはいけない。そのための仕掛けがあるはず。
一方、チャネルは濃度の濃い方から薄い方へと物質が流れるのをゲートを開けたり閉じたりして制御する孔と言えます。流れの方向は物質の濃度差で決まっているので、チャネルのゲートの仕事は単にその流れを止めるか許すかであり、ゲートは基本的に一つあれば足ります。神経が興奮するとこのゲートが開いて細胞の外からNa+が細胞内へと流入します。神経が興奮すると電気信号が出ますが、電気信号の実体はこのNa+イオンの流れです。パリトキシンはNKAをNa+、K+に限らずもっと大きいイオンでも陽イオンならほぼ何でも通すチャネルに変えてしまいます。要するに膜蛋白質に孔を開けてしまうわけです。その結果、細胞内に大量のNa+が流れ込み、異常興奮の状態になって細胞を壊してしまいます。
それでは、ポンプ蛋白質はチャネル蛋白質にもう一つゲートが付け加えられたものと考えてよいでしょうか?パリトキシンは二つあるゲートのどちらかが閉まらないようにしてしまうのでしょうか、開閉の順番を変えてしまうのでしょうか。それとも、本来のイオン通路の他に新たな通路を作るのでしょうか。それに答えるのが本研究の科学的眼目です。その最も直接的な方法は、パリトキシンを結合したNKAの立体構造を原子レベルで決定することです。
今回PNAS誌に発表した論文ではイオンポンプを代表する「ナトリウム・カリウムポンプをパリトキシンはどのようにして陽イオンチャネルに変えてしまうか」を、クライオ電子顕微鏡法を使って決定した原子構造に基づいて記述しています(図1)。これは、ポンプとチャネルがどう違うのか、或いは同じなのかを明らかにするものとして長く待ち望まれていた構造研究です。
2.パリトキシンとNKAの複合体の構造
パリトキシンは細胞の外からNKAに結合しますから、細胞外側ゲートが開いた状態(E2P状態)に結合します(図1左)。細胞外側ゲートが開くとイオン結合部位まで長くて真っ直ぐな通路ができます。ここの通路にパリトキシンのプラグと名付けた部分(用語解説参照)が深く挿入されていました。NKAは実は強心ステロイドと呼ばれる強心剤の標的蛋白質です。栽培する人もいるジギタリスが有名で、「魔女の薬」と呼ばれて18世紀から処方されてきました。面白いことに、パリトキシンのプラグ部分の結合はistaroximeと呼ばれる新世代の強心剤とよく似ていました。確かに構造も似ています。ですが、この状態では細胞外側のイオン通路はパリトキシンによって拡張されていますが、膜を貫通するチャネルはできていませんでした(図1中央)。つまり、パリトキシンは細胞外側イオン通路に入りこみ孔を広げるけれども、細胞内側ゲートを開ける能力は無いということです。
そこで、細胞内側のゲートを開けるのに必須なATP(アデノシン三燐酸)とNa+を加えてみました。そうしたら期待通りに、膜を貫通する通路(チャネル)ができていました図1右)。途中の狭いところは負の電荷を持つアミノ酸残基に囲まれていたので、陽イオンしか通さないこともわかりました。NKAは生理的状態で一度に3個のNa+イオンを運搬できるのですが、驚いたことに、少なくとも2個のNa+はしっかり結合していました。また、パリトキシンによって誘導されたイオン通路は生理的な通路の脇にバイパスのように作られていました。本来、細胞内側のゲートが開くときには細胞外側の通路は消失するようにNKAは構造を変えるのですが、その通路はパリトキシンが埋めてしまっているために、NKAは本来起こすべき構造変化を起こせない。だけれども、細胞内側ゲートを開けるための構造変化はできてしまう。そういう異常事態が起こっていたわけです。そして、そのバイパスの壁をパリトキシンが作っていてNKA側の動きに応じてパリトキシンも蛇腹のように伸び縮みし、壁が壊れないようにしていました。パリトキシンには沢山の水酸基がありますが(用語解説参照)、それはイオンを通すためだったのです。つまり、本来は細胞内側ゲートを開けるのと細胞外側通路を閉じてしまう動作(構造変化)の間には緊密な連携があるのですが、パリトキシンはその連携を壊していたということです。
3.イオンポンプとチャネルの本質的違い
この結果、NKAで代表されるイオンポンプの場合、「ゲートを開閉する」というけれども、それは孔に付けられた弁を開け閉めするのではなく、イオン通路そのものを破壊・生成するというサイクルを繰り返していることがわかりました(図3)。概念的にはイオン通路の両側に弁があれば良さそうです。イオンチャネルがもう一つゲートを持てば良さそうです。でも、そうはなっていないのです。どうしてでしょうか?それはセキュリティのためと考えられます。NKAの場合は数十倍、カルシウムポンプに至っては1万倍以上の濃度差を維持しなければなりません。常に孔が存在しそれに弁が二つついていれば開閉に必要な構造変化は小さいだろうから、速い応答が可能です。ですが、蛋白質は~37℃という比較的高温環境にありますから、常に熱運動でふらふらしています。そのために、チャネルの場合、どうしてもある確率で勝手に開いてしまうことが起こります。それではイオンの濃度差は失われてしまい、ポンプはその役割を果たせません。ですから、ゲートを閉めるときには通路自体をなくしてしまう、ということをしているのでしょう。つまり、チャネルとポンプは果たすべき役割が違い、それに応じて蛋白質のデザインの方針も違うということが、今回の研究で明らかになった(サイエンスとして)重要なポイントです。
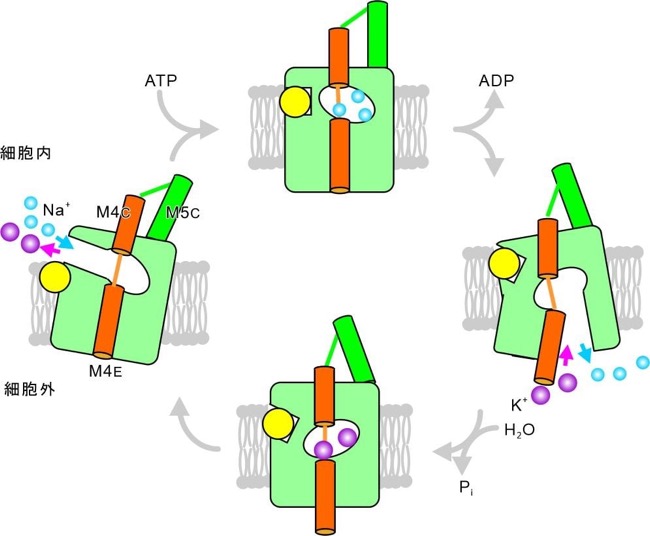
図3:実際のナトリウム・カリウムポンプの作動機構
ナトリウム・カリウムポンプのイオン通路は細胞内側と外側の大きく性質の違う二つの部分から成っていて、二つの部分は同時には存在しないことが分かった。弁のようなゲートを開け閉めするのではなく、通路全体を生成・破壊するというサイクルを繰り返すのである。
構造変化を理解するには動画を見るのが一番ですので、是非、下記動画をご覧ください。
発表者・研究者等情報
東京大学定量生命科学研究所豊島 近特任教授 (東京大学特別教授)
金井 隆太 特任講師
恒川 直樹 特任研究員
オルフス大学 生命医学部(デンマーク)
Flemming Cornelius 博士
Bente Vilsen 教授
研究助成
本研究は、科研費「基盤研究B(課題番号:23K27136)」、「基盤研究B(課題番号:24K01985)」の支援により実施されました。用語解説
1.パリトキシンについてパリトキシン(Palytoxin)は、イワスナギンチャク(Palythoa)などにに共生する有毒渦鞭毛藻が産生し、食物連鎖によって魚類(アオブダイ、ハコフグ、ソウシハギなど)に蓄積されます。生物界最強の毒物の一つで、毒の強さは青酸カリの数万倍、フグの毒(テトロドトキシン)の約60~70倍という報告もあります。ハワイの先住民族では、矢毒として用いられていたそうです。
我が国におけるパリトキシンによると考えられる食中毒に関しては厚労省ホームページ(https://www.mhlw.go.jp/topics/syokuchu/poison/animal_det_03.html)に詳しい記述があります。アオブダイの摂食によるものが広く知られており、その他、クエ、ハコフグ、ウミスズメ、ソウシハギなどの報告があります。鹿児島、宮崎、高知など九州、四国で多く発生しています。1953年から2024年にかけて、少なくとも48件の中毒の記録があり、患者総数は148名、そのうち8名が死亡しています。最近では2023年12月に報告が有り、2020年11月には14人の集団中毒がありました。横紋筋の融解に由来する激しい筋肉痛(横紋筋融解症)が主症状で、 冠状動脈が極度に収縮し、死に至ることもあります。解毒剤はなく、しかも、加熱しても毒性は失われません。
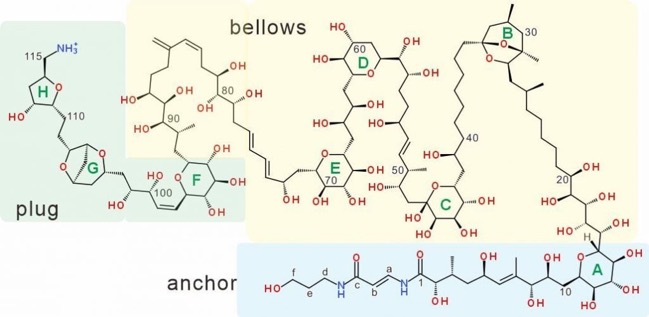
上図のように非常に複雑な分子であり「作用機構は不明であるが」とホームページではなっていますが、今回の研究で解明されたわけです。また、機能的には三つの部分から成ることが今回の研究で判明しました。また、パリトキシンの全合成は1994年にハーバード大学の岸義人教授グループによって成され、現在でも有機合成化学における金字塔とされています。
2.ナトリウム・カリウムポンプについて
ナトリウム・カリウムポンプ(Na+,K+-ATPase、NKA)はATP(アデノシン三燐酸)がADP(アデノシン二燐酸)と燐酸に分解されるときに放出されるエネルギーを利用して、1分子のATPの分解当たり3個のNa+を細胞内から細胞外へ、2個のK+を細胞外から細胞内へと細胞膜を越えて運搬する膜蛋白質です。ほぼすべての動物細胞に発現している極めて重要な蛋白質です。このポンプが止まってしまうと、神経興奮は無くなってしまいます。ATPを分解するのでATPase(ATPアーゼ)と呼ばれる酵素でもあります。厳密にNa+を選択して細胞内から外へと運搬しますが、逆方向の選択性は厳しくなく、Na+だけでも反応サイクルは回ります。そのため、ナトリウムポンプと言われることもあります。実際、今回の研究ではNa+だけが使われています。酵素活性を持つαサブユニットは約1,000残基のアミノ酸からなり、3つの明瞭に分離した細胞質ドメインと10本(M1-M10)の膜貫通へリックスから成る、比較的大型の蛋白質です。特に重要なのは背骨となっているM5へリックスと手押しポンプのピストンのような役割をするM4へリックスです。
アイキャッチ画像
雑誌名等
雑誌名:Proceedings of the National Academy of Sciences of United States of America題 名:How palytoxin transforms the Na+,K+ pump into a cation channel
著者名:Ryuta Kanai, Naoki Tsunekawa, Flemming Cornelius, Bente Vilsen and Chikashi Toyoshima*(*責任著者)
DOI:10.1073/pnas.2506450122.
URL:www.pnas.org/doi/10.1073/pnas.2506450122
問い合わせ先
研究内容については発表者にお問い合わせください東京大学定量生命科学研究所
特任教授 豊島 近(とよしま ちかし)
Tel:03-5841-8492 E-mail:ct@iqb.u-tokyo.ac.jp
東京大学定量生命科学研究所 総務チーム
Tel:03-5841-7813 E-mail:soumu@iqb.u-tokyo.ac.jp
 東京大学 研究
東京大学 研究