抗サイトメガロウイルス薬「バルガンシクロビル」の先天性サイトメガロウイルス感染症の遅発性難聴への医師主導治験を開始
【産学連携対象 全学共通分野 Discovery Saga】
【持続可能な開発目標(SDGs)】
【Sagaキーワード】
エステル/持続可能/持続可能な開発/病原微生物/周波数/微生物/エイズ/聴性脳幹反応(ABR)/精子形成/免疫不全/ウイルス感染症/幹細胞移植/聴覚/難聴/免疫抑制/聴覚障害/悪性腫瘍/骨髄/細胞移植/造血幹細胞/スクリーニング/プロドラッグ/ヘルペスウイルス/幹細胞/血小板/好中球/細胞・組織/精子/副作用/ウイルス/医師/感染症/細菌/小児/新生児/臓器移植/造血/造血幹細胞移植/動物実験/乳幼児/臨床研究
2025.08.26
概要
この度、日本大学医学部小児科 森岡一朗教授、埼玉県立小児医療センター 岡明病院長、神戸大学医学部附属病院小児科 野津寛大教授、国立成育医療研究センター 守本倫子診療部長らの研究グループは、神戸大学医学部附属病院臨床研究推進センターを治験事務局として、臨床研究・治験推進研究事業・「先天性サイトメガロウイルス(CMV)※1 感染児の遅発性難聴を対象としたバルガンシクロビル塩酸塩ドライシロップの有効性および安全性を評価する多施設共同プラセボ対照ランダム化並行群間比較試験(VGCV-3)」医師主導治験を開始しました。本治験は、令和7年3月から神戸大学医学部附属病院、日本大学医学部附属板橋病院で開始され、以降、全国17施設の医療機関において順次治験が開始されています。
なお、この治験は、日本医療研究開発機構(AMED)「臨床研究・治験推進研究事業」の支援を受けています。
先天性サイトメガロウイルス感染症について
先天性サイトメガロウイルス(CMV)感染症は、CMVの母子感染(※2)によって、聴覚障害、発達遅延等の重い後遺症を残す可能性がある、最も発生頻度の高い先天性感染症です。我が国の年間総出生児の0.3%(約2700人/90万人出生)が先天性CMV感染を伴って出生しており、この先天性CMV感染症は、その後に難聴や発達遅延を生じており、我が国の小児に大きな疾病負荷を与えています。バルガンシクロビルの有効性および安全性を評価する医師主導治験
抗CMV薬であるバルガンシクロビルを生後早期から投与することにより、聴力障害や発達遅延の治療、または症状進展を抑制しうることが、我が国や諸外国の臨床研究で示されています。CMVに対する代表的な治療薬として、経口投与可能なバルガンシクロビル(※3)があり、われわれが行った医師主導治験により、生後2か月以内の症候性先天性CMV感染症に対する保険適応が認められています。現在、日本では生後3週以内の新生児尿を用いた先天性CMV感染の診断が一般診療で可能となっており、症候性先天性CMV感染症に対しては本薬の保険承認下での使用が行われています。一方で、先天性CMV感染症で出生時に聴力障害はなかったが遅発性に難聴を発症した乳幼児や、原因不明の難聴で乳幼児期にCMV感染症が判明した児に対する保険適応はありません。
本治験では、先天性CMV感染症の遅発性難聴の方を対象とし、バルガンシクロビル経口液剤(バルガンシクロビル塩酸塩ドライシロップ)治療の第II相多施設共同プラセボ対照二重盲検比較医師主導試験(※4, ※5)を行います。
治験の概要
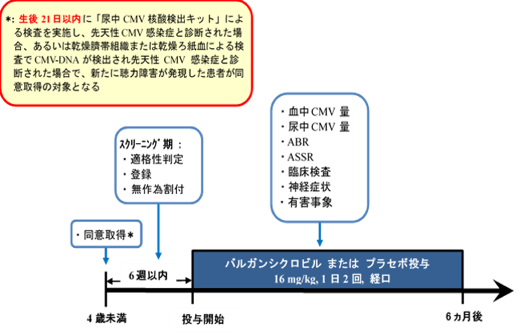
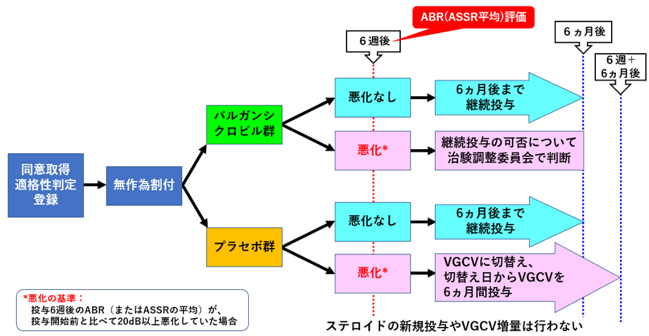
本治験は、選択基準(表1)を満たす先天性CMV感染児の遅発性難聴を対象に、被験者の代諾者から文書により同意を取得した後に、バルガンシクロビル1回16 mg/kgを1日2回経口投与します。投与期間は6か月間とし、投与6か月後に定められた効果判定を行い、投与終了1ヵ月後まで観察・検査を行います(図1)。6週後に難聴が進行している場合には、開鍵し、プラセボの場合にはバルガンシクロビルを投与します(図2)。治験の評価項目は以下のとおりです。
a. 主要評価項目ベースライン時点の聴性脳幹反応(ABR)または聴性定常反応(ASSR)に基づき軽度以上の聴力障害を有するTotal earにおける、治験薬投与開始6ヵ月後の「聴力改善」の有無b. 副次評価項目1)ベースライン時点のABRまたはASSRに基づき軽度以上の聴力障害を有するTotal earにおける、治験薬投与開始6週後の「聴力改善」の有無
2)治験薬投与開始6週後および6ヵ月後の聴力障害レベルについて、ABRまたはASSRに基づくBest response earにおける、「聴力改善」の有無
3)治験薬投与開始6週後および6ヵ月後の聴力障害レベルについて、ABRに基づくTotal earにおける、「聴力改善」の有無、「改善+不変」の有無、ABR出現レベル(dB)の変化量
4)治験薬投与開始 6週後および6ヵ月後の聴力障害レベルについて、ABRに基づくBest responseearにおける 、「聴力改善」の有無、「改善+不変」の有無、ABR出現レベル(dB)の変化量
5)ASSRに基づく各周波数の聴力障害レベルについて、ABRの上記3および4と同様の項目
6)全血中CMV量
7)血漿中CMV量
8)尿中CMV量
9)ベースラインで認められた血小板数減少、肝機能障害の改善
10)有害事象および副作用
2)治験薬投与開始6週後および6ヵ月後の聴力障害レベルについて、ABRまたはASSRに基づくBest response earにおける、「聴力改善」の有無
3)治験薬投与開始6週後および6ヵ月後の聴力障害レベルについて、ABRに基づくTotal earにおける、「聴力改善」の有無、「改善+不変」の有無、ABR出現レベル(dB)の変化量
4)治験薬投与開始 6週後および6ヵ月後の聴力障害レベルについて、ABRに基づくBest responseearにおける 、「聴力改善」の有無、「改善+不変」の有無、ABR出現レベル(dB)の変化量
5)ASSRに基づく各周波数の聴力障害レベルについて、ABRの上記3および4と同様の項目
6)全血中CMV量
7)血漿中CMV量
8)尿中CMV量
9)ベースラインで認められた血小板数減少、肝機能障害の改善
10)有害事象および副作用
| 生後21日以内に実施した尿中CMV核酸検出キットで先天性CMV感染症と診断された患者、あるいは、乾燥臍帯組織または乾燥ろ紙血による検査でCMV-DNAが検出され先天性 CMV 感染症と診断された患者 |
| treraut出生時は無症候性で生後21日以後に遅発性難聴を呈した患者、または出生時に症候性であっても聴覚障害を認めておらず、その後に遅発性難聴を呈した患者 |
| 遅発性難聴の障害の程度が、少なくとも片耳で30 dB以上90 dB以下の範囲に含まれている患者(スクリーニング時) |
| 満4歳未満(同意取得時) |
| 本治験への登録前に治験の内容について十分な説明を行い、治験への参加に代諾者から文書による同意が得られた患者 |
表1. 選択基準
 神戸大学 研究
神戸大学 研究

