気孔を閉じさせるK+チャネルの調節部位を発見
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
オープンアクセス/検索システム/環境変化/幾何学/円二色性/分子構造/タンパク質凝集/ホウ酸/円偏光/加水分解/水分解/持続可能/二次構造/3次元構造/カリウム/ポリマー/電子顕微鏡/電子顕微鏡観察/分解能/リン酸/病原菌/シロイヌナズナ/環境ストレス/バイオマス/加水分解酵素/結晶性/キチン/クライオ電子顕微鏡/病原体/WT1/シャペロン/細胞膜/脂質二重膜/ゆらぎ/心臓/生理機能/イオンチャネル/イミン/コンフォメーション/ヘリックス/構造変化/生体分子/電気生理学/膜タンパク質/膜電位/立体構造/ストレス/脂質/生理学
2025年7月25日 公開
ポイント
植物の気孔閉鎖を誘導するカリウムイオンチャネル[用語1]であるGORK[用語2]の立体構造を明らかにしました。イオンチャネルの開閉を制御する部位を新たに特定しました。
GORKは乾燥や病原菌の侵入に対する植物の防御反応に関与しており、その実態が明らかになりました。
本成果は、気孔閉鎖を誘導する生物刺激剤(バイオスティミュラント)開発など、農業応用への展開が期待されます。
概要
植物は、気孔の開閉を通じて水分の蒸散を調節し、乾燥や病原菌などの環境ストレスに応答しています。気孔の開閉は、2つの孔辺細胞の膨張と収縮によって生じ、この膨圧変化は細胞内の主要元素であるカリウムイオン(K+)の濃度に依存しています。K+の細胞内外への移動は、細胞膜に存在するK+チャネルによって制御されており、その働きが気孔の開閉に重要な役割を果たしています。東北大学を中心とした国際共同研究チームは、K+チャネルの一種であるGORKの分子構造をクライオ電子顕微鏡(Cryo-EM)[用語3]を用いて高精度に決定しました。さらに、GORKチャネルの活性化と不活性化状態を制御する領域を、電気生理学的測定[用語4]およびCircular Dichroism[用語5]を用いた解析によって明らかにしました。
本研究における構造と機能の解析は、東北大学 大学院工学研究科 バイオ工学専攻の村岡勇樹学術研究員、山梨太郎大学院生、石丸泰寛准教授、魚住信之教授らによって行われました。加えて、同大学 大学院生命科学研究科の田中良和教授、横山武司助教、東京科学大学 生命理工学院 生命理工学系の古田忠臣助教、東北大学 大学院工学研究科バイオ工学専攻の梅津光央教授、中澤光准教授、伊藤智之助教、チリ・タルカ大学のIngo Dreyer教授、米国カリフォルニア大学 サンディエゴ校のJulian Schroeder教授による共同研究による成果です。
本研究の成果は、2025年7月23日(米国東部時間)に米国科学アカデミー紀要「Proceedings of the National Academy of Sciences(PNAS)」にオンラインで掲載されました。
背景
植物の気孔は、外界の環境変化に応じて開閉し、水分保持や病原体の侵入防止といった生理機能を果たしています。気孔の開閉を制御する孔辺細胞は、K+の流出によって膨圧が低下し、気孔が閉じることが知られています。特に、モデル植物シロイヌナズナにおいて、外向き整流性K+チャネルGORKは、気孔閉鎖を促進する重要な因子として注目されてきました。しかし、GORKの構造やK+輸送活性の詳細な制御機構は、これまで解明されていませんでした。今回の取り組み
本研究では、クライオ電子顕微鏡を用いて、GORKチャネルの5つの異なる構造状態(コンフォメーション)を、3.16〜3.27 Åの分解能で解析しました。GORKは、膜貫通領域に加え、細胞質側に環状ヌクレオチド結合ドメイン(cyclic nucleotide-binding domain, CNBD)およびアンキリン領域(ankyrin repeat)を有し、これらのドメインは、CNBD–Ankyrin bridgeによって連結されていました。解析の結果、このCNBD–Ankyrin bridgeは、GORKチャネルの開閉状態に応じて構造が変化することが分かりました。具体的には、チャネルが活性化されたPre-open状態ではαヘリックス構造を、不活性なClosed状態ではループ構造をとっており、この構造変化がGORKの開閉制御に関与していると考えられます(図1)。また、リン酸化や細胞質pHの変化がこの構造変化を引き起こす要因となっている可能性が明らかになりました。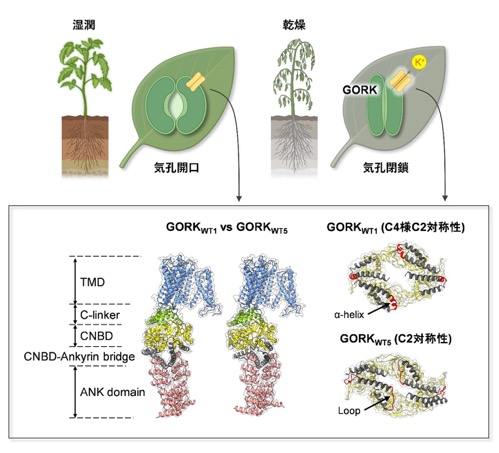
今後の展開
今回の成果は、植物の気孔制御メカニズムを分子レベルで明らかにするうえで、重要な一歩となるものです。GORKチャネルの立体構造と、その開閉を制御する構造変化が明らかになったことで、今後はこの知見をもとに、気孔閉鎖を人為的に誘導する生物刺激剤(バイオスティミュラント)の開発や、乾燥や病原菌に対する植物の耐性を高める作物の育種など、農業分野への応用が期待されます。また、GORKを標的とした制御技術の確立は、環境ストレスに強い植物の設計にもつながる可能性があり、持続可能な農業の実現に向けた新たな展開が望まれます。付記
本研究は、科学研究費助成事業(JP21H05266,JP21KK0268,JP22K19121,JP23KJ0172,JP24K17825,JP24K23201,JP24H00295,JP24H02253,JP24H00495,JP23K138620)、JSTムーンショット型研究開発事業(JPMJMS2033)、NSF(MCB-2401310)、ANID(Ingo Dreyer 1220504)の支援を受けました。用語説明
- [用語1]
- イオンチャネル:細胞膜を横断してイオンを透過する膜タンパク質。
- [用語2]
- GORK:孔辺細胞からK+を排出するKチャネル。動物の神経・心臓で機能する膜電位依存性K+チャネルと同じ仲間。Guard cell Outward Rectifying K+ channels。
- [用語3]
- クライオ電子顕微鏡(Cryo-EM):生体分子を急速凍結し低温環境で電子顕微鏡観察を行う手法。
- [用語4]
- 電気生理学的測定:イオンチャネルのイオン電流を実測する測定法。
- [用語5]
- Circular Dichroism(CD, 円二色性):左右の円偏光の吸収の差を測定する方法。タンパク質の二次構造(αへリックスなど)の含量の解析に用いる。
論文情報
- 掲載誌:
- Proceedings of the National Academy of Sciences (PNAS)(オープンアクセス)
- タイトル:
- Structure reveals a regulation mechanism of plant outward-rectifying K+ channel GORK by structural rearrangements in the CNBD–Ankyrin bridge
- 著者:
- Taro Yamanashi*, Yuki Muraoka*, Tadaomi Furuta, Tsukasa Kume, Natsuko Sekido, Shunya Saito, Shota Terashima, Takeshi Yokoyama, Yoshikazu Tanaka, Atsushi Miyamoto, Kanane Sato, Tomoyuki Ito, Hikaru Nakazawa, Mitsuo Umetsu, Ellen Tanudjaja, Masaru Tsujii, Ingo Dreyer, Julian I. Schroeder, Yasuhiro Ishimaru, and Nobuyuki Uozumi(山梨太郎*,村岡勇樹*,古田忠臣,久米司,関戸菜津子,寺島照太,齋藤俊也,横山武司,田中良和,宮本敦史,佐藤奏音,伊藤智之,中澤光,梅津光央,Elen Tanujaja,辻井雅,Ingo Dreyer,Julian I. Schroeder,石丸泰寛,魚住信之**)(*筆頭著者)
**責任著者:東北大学大学院工学研究科 教授 魚住信之 - DOI:
- 10.1073/pnas.2500070122
関連リンク
プレスリリース 気孔を閉じさせるK+チャネルの調節部位を発見(PDF)タンパク質カゴ内に「金属ゼロ」の触媒を創出|Science Tokyoニュース
令和6年度 手島精一記念研究賞の受賞者決定|Science Tokyoニュース
ふらふらな分子を止めて構造を見るタンパク質の「組木細工」|旧・東京工業大学
Aqp10タンパク質の尿素・ホウ酸輸送活性の減弱が生じた進化上のタイミングを同定|旧・東京工業大学
細胞と細胞をつなぐ分子の結合過程の撮影に成功|旧・東京工業大学
世界最小サイズの発光酵素picALuc®の開発に成功|旧・東京工業大学
革新的ポリマーを用いたタンパク質凝集阻害メカニズムの解明|旧・東京工業大学
動いて並んでつながって。タンパク質が幾何学模様に!|旧・東京工業大学
人工シャペロンにより脂質二重膜の2次元/3次元構造の高効率で可逆的な変換に初めて成功|旧・東京工業大学
キチン加水分解酵素は熱ゆらぎを利用して一方向に動きながら結晶性バイオマスを分解する分子モノレールカーである|旧・東京工業大学
古田 忠臣 Tadaomi Furuta|研究者検索システム Science Tokyo STAR Search
生命理工学院 生命理工学系
生命理工学院
東北大学 工学研究科・工学部
東北大学 大学院生命科学研究科
タルカ大学
カリフォルニア大学 サンディエゴ校
取材申込みフォーム
問い合わせ先
東北大学大学院工学研究科バイオ工学専攻教授 魚住信之
- Tel
- 022-795-7280
- uozumi@tohoku.ac.jp
東京科学大学 生命理工学院
助教 古田忠臣
- Tel
- 045-924-5776
- furuta@bio.titech.ac.jp
取材申込み
東北大学大学院工学研究科情報広報室担当 沼澤みどり
- Tel
- 022-795-5898
- eng-pr@grp.tohoku.ac.jp
東京科学大学 総務企画部 広報課
- Tel
- 03-5734-2975
- Fax
- 03-5734-3661
- media@adm.isct.ac.jp
 東京科学大学 研究
東京科学大学 研究