破骨細胞分化を促すシグナル「RANK-RANKL結合」の可視化に成功
【産学連携対象 全学共通分野 Discovery Saga】
【Sagaキーワード】
高齢化社会/検索システム/中性子/タンパク質間相互作用/ナノ空間/可視化技術/酵素活性/細胞間コミュニケーション/悪性脳腫瘍/染色体/破骨細胞分化/骨折/寿命/障害者/分子標的/リハビリ/間葉系細胞/骨細胞/骨密度/細胞融合/歯学/前駆細胞/in vitro/RANKL/スクリーニング/タンパク質相互作用/ファージ/マクロファージ/ルシフェラーゼ/遺伝子導入/化合物ライブラリー/構造活性相関/骨芽細胞/骨吸収/骨形成/骨粗鬆症/骨代謝/細胞分化/受容体/阻害剤/低分子化合物/破骨細胞/誘導体/コミュニケーション/リハビリテーション/遺伝子/遺伝子変異/加齢/健康寿命/高齢化/高齢者/脳腫瘍/分子標的治療/分子標的治療薬/網羅的解析
2025年4月9日 公開
骨粗鬆症の新たな治療薬開発を目指して
ポイント
骨密度低下は、骨吸収が骨形成を上回ることで生じます。本研究では、RANK-RANKL結合をin vitroで可視化する手法を樹立しました。大理石骨病の原因となる遺伝子変異が、RANK-RANKL結合の親和性低下によることを確認しました。
可視化技術を用いたスクリーニングで、骨粗鬆症治療薬の候補となる新規化合物を発見しました。
概要
東京科学大学(Science Tokyo)大学院医歯学総合研究科 分子細胞機能学分野の中濵健一准教授と同 総合研究院 化学生命科学研究所の中村浩之教授、および国立障害者リハビリテーションセンターらの研究チームは、NanoBiT技術[用語1]を用いてRANK-RANKL結合[用語2]を発光によって可視化することで、生きた細胞における結合場所の特定および定量化に成功しました。骨は、骨を合成する骨芽細胞と、骨を溶かす破骨細胞によって常に新しく作り替えられ、骨の強度が保たれています。骨が弱くなる骨粗鬆症では、破骨細胞による骨吸収量の増加が原因であることが知られています。破骨細胞は、RANKを発現する単球系の細胞がRANKLによる刺激を受けて分化することから、RANK-RANKL結合の可視化技術は、破骨細胞の分化機構の解明や骨粗鬆症の治療薬探索において重要であると考えられます。
本技術を用いた実験の結果、常染色体劣性骨硬化症(ARO)患者の一部に見られる遺伝子変異では、RANK-RANKL結合が正常に起こらず、疾患が発症することが確認されました。さらに、本技術を用いてin-houseの3次元骨格低分子化合物ライブラリーのスクリーニングを行ったところ、一つの分子がRANK-RANKL結合を阻害し、破骨細胞の分化を抑制することが明らかとなりました。
本研究によって得られた化合物は、今後の骨粗鬆症薬開発におけるリード化合物となる可能性が示されました。
本成果は、現地時間3月28日付で「Bone」誌にオンライン掲載されました。
背景
超高齢化社会を迎えた現在、老後の健康をいかに維持するかは大きな課題となっています。加齢に伴い骨密度は低下し、高齢者における骨折は寝たきりにつながるリスクが高まります。したがって、健康寿命を維持するためには、骨密度の低下を予防・治療することが重要です。骨密度の低下は、骨代謝において骨形成を骨吸収が上回ることによって生じます。この骨吸収を担っているのが破骨細胞です。破骨細胞は、破骨細胞分化因子(RANKL)の刺激を受けたマクロファージ系の細胞が細胞融合し、多核の強大な細胞へと分化した、骨に特異的な細胞です。
そこで本研究チームは、RANK(RANKL受容体)-RANKLの結合を、生きた細胞で可視化・定量化できる実験系の構築を試みました。
研究成果
近年、生きた細胞でタンパク質相互作用を検出する技術が確立されており、中でもNanoBiT技術は、タンパク質相互作用を高感度に検出できる手法として注目されています。本研究チームは、この技術を応用し、RANK-RANKL結合の可視化および定量化に成功しました。大理石骨病は希少疾患ですが、RANKまたはRANKL遺伝子に変異がある患者に見られる変異を遺伝子導入することによって再現することで、破骨細胞が形成されない原因がRANK-RANKL結合の不全によることを明らかにすることができました。
さらに、in-houseで保有する3次元骨低分子化合物ライブラリーを用いてスクリーニングを行った結果、RANK-RANKL結合の新規阻害剤「CRL71-355」を見出すことに成功しました。
社会的インパクト
本論文の研究成果は、RANK-RANKL結合に関連する疾患の発見や、骨代謝異常疾患のメカニズム解明に寄与すると考えられます。さらに、低分子化合物を用いたスクリーニングにより、新規化合物による骨粗鬆症治療薬の開発にも貢献できると期待されます。今後の展開
1. RANK-RANKL結合を生きた細胞で経時的に観察できる実験系を開発したことにより、破骨細胞の分化に伴うRANK-RANKL結合の局在変化などについて、さらに研究を進めていきたいと考えています。2. RANK-RANKL結合阻害剤であるCRL71-355については、その作用部位の特定を進め、安全性および薬効に優れた誘導体の開発へとつなげていきます。
付記
本研究は、科学研究費助成事業(JP24K12866ZA)の支援を受けて行われました。用語説明
- [用語1]
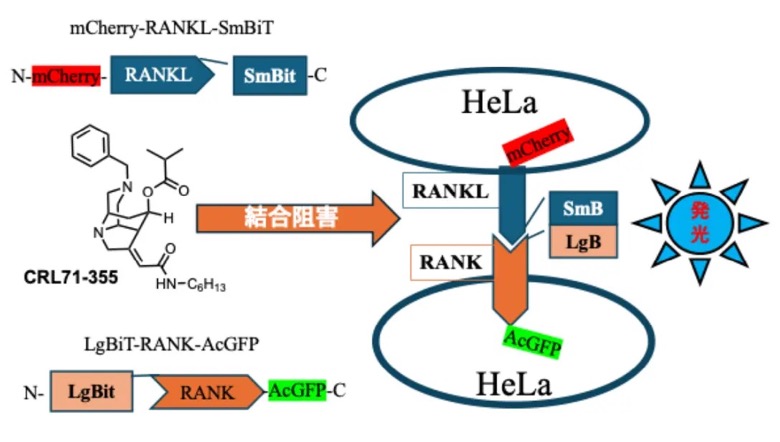
- NanoBiT(NanoLuc® Binary Technology):タンパク質間相互作用を光信号として検出する技術。プロメガ社が開発したこの技術では、ルシフェラーゼ活性を持つ酵素を二つの部分(LgBとSmB)に分け、それぞれを異なるタンパク質に融合させる。相互作用によりLgBとSmBが会合すると、酵素活性が再構成されて発光を生じるシステムである。
- [用語2]
- RANK- RANKL結合:RANK(Receptor activator of NFκB)は、破骨細胞に分化する前の前駆細胞に発現している受容体である。RANKL(receptor activator of NFκB ligand)は、間葉系細胞に発現している破骨細胞分化因子であり、RANKと結合することで破骨細胞の分化を促進する。RANK-RANKL結合は、骨を溶解する破骨細胞の形成に不可欠な分子間相互作用である。
論文情報
- 掲載誌:
- Bone
- タイトル:
- Visualization and quantification of RANK-RANKL binding for application to disease investigations and drug discovery
- 著者:
- Ken-ichi Nakahama, Shiho Hidaka, Kanako Goto, Mayu Tada, Tomoya Doi, Hiroyuki Nakamura, Masako Akiyama, Masahiro Shinohara
- DOI:
- 10.1016/j.bone.2025.117473
研究者プロフィール
中濵 健一 Ken-ichi NAKAHAMA
東京科学大学 大学院医歯学総合研究科 分子細胞機能学分野 准教授
研究分野:骨代謝と細胞間コミュニケーション

中村 浩之 Hiroyuki NAKAMURA
東京科学大学 総合研究院 化学生命科学研究所 教授
研究分野:分子標的治療薬剤の設計および合成

関連リンク
プレスリリース 破骨細胞分化を促すシグナル「RANK-RANKL結合」の可視化に成功—骨粗鬆症の新たな治療薬開発を目指して—(PDF)光で骨吸収をコントロールする新技術を開発|旧・東京医科歯科大学
難治性悪性脳腫瘍の中性子捕捉治療に有望な薬剤の開発|旧・東京工業大学
“構造活性相関転移”による低分子医薬品候補の設計|旧・東京工業大学
ナノ空間で制御可能なヒスチジン残基化学修飾を開発|旧・東京工業大学
膨大な活性データの網羅的解析から低分子医薬品候補を創出|旧・東京工業大学
中濵 健一 Ken-ichi Nakahama|Science Tokyo 研究情報データベース
中村 浩之 Hiroyuki Nakamura|研究者検索システム Science Tokyo STAR Search
中村・岡田研究室
分子細胞機能学分野
大学院医歯学総合研究科|旧・東京医科歯科大学
総合研究院 化学生命科学研究所
生命理工学院 生命理工学系
総合研究院
生命理工学院
医歯学総合研究科
国立障害者リハビリテーションセンター
取材申込みフォーム
お問い合わせ
東京科学大学 大学院医歯学総合研究科 分子細胞機能学分野准教授 中濵 健一
- Tel
- 03-5803-5574
- Fax
- 03-5803-0212
- nakacell@tmd.ac.jp
取材申込み
東京科学大学 総務企画部 広報課- Tel
- 03-5734-2975
- Fax
- 03-5734-3661
- media@adm.isct.ac.jp
 東京科学大学 研究
東京科学大学 研究