がん抑制遺伝子ARID1Aのゲノム安定性における新たな機能の発見
【産学連携対象 全学共通分野 Discovery Saga】
【持続可能な開発目標(SDGs)】
【Sagaキーワード】
化学物質/タンパク質間相互作用/持続可能/紫外線/持続可能な開発/モデリング/アミノ酸配列/DNA二本鎖切断/クロマチンリモデリング/DNA修復/クロマチン/ゲノム安定性/ゲノム不安定性/腫瘍学/がん化/リモデリング/DNA損傷/DNA複製/RNA/アミノ酸/がん抑制遺伝子/活性酸素/構造変化/細胞核/細胞死/ゲノム/遺伝子/遺伝子発現/化学療法/加齢/放射線
2025年4月 2日 14:00
研究者情報
〇加齢医学研究所 分子腫瘍学研究分野 准教授 宇井彩子発表のポイント
発表概要
ARID1Aは多種多様ながんで高頻度に変異していますが、その機能とがん化抑制機能のメカニズムはまだ完全に解明されていません。東北大学加齢医学研究所分子腫瘍学研究分野の菅野新一郎講師、小林孝安准教授、田中耕三教授、安井明学術研究員、宇井彩子准教授らは、クロマチン(注4)の構造変化を促すクロマチンリモデリング(注5)複合体におけるARID1Aの新たなタンパク質間相互作用のネットワークを明らかにし、それらのタンパク質の中にARID1Aとの結合に関与する保存されたアミノ酸配列を見出しました。これらARID1Aの相互作用因子の中で、DNA二重鎖切断の修復に関わる因子との相互作用を新たに発見し、その機能的な意義を明らかにしました。DNA二重鎖切断は致死的なDNA損傷であり、その修復異常はゲノム不安定性を引き起こし、細胞のがん化に関わると考えられています。
今回の発見から、ARID1Aが有するゲノム安定性(注6)維持機構における新たな機能とそのメカニズムが明らかになりました。
本研究成果は、2025年3月13日に学術誌 Nucleic Acids Research誌で発表されました。
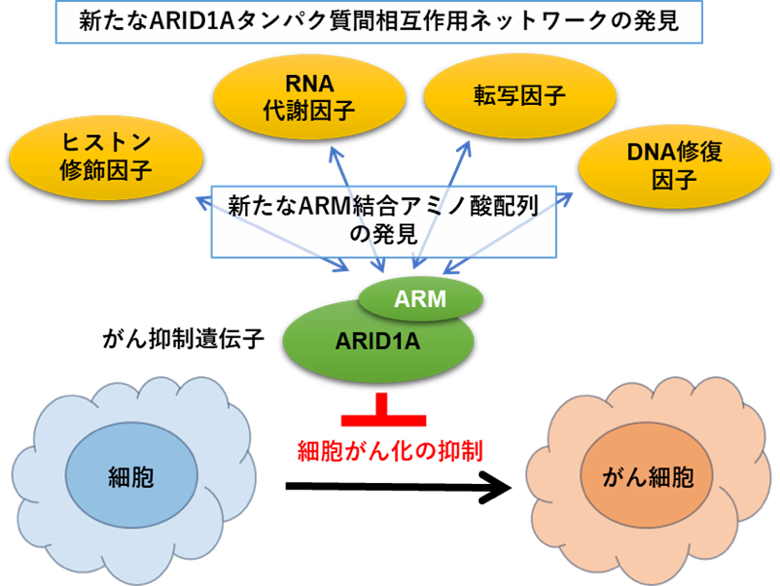
図1. 本研究のイメージ図
用語解説
注1. DNA修復とは、細胞がDNAの損傷を修復する仕組みです。DNAの損傷は、紫外線や化学物質、活性酸素や放射線などによって引き起こされます。注2. ゲノム不安定性とは、DNA(ゲノム)の修復機能に異常が生じ、変異が起こりやすい状態を指し、がんの特徴の一つです。
注3. DNA二本鎖切断の修復(DNA double strand break; DSB)とは、DNA損傷の中でも特に致死的なDNAの二重鎖が切断された損傷を修復する仕組みです。放射線や活性酸素、がん化学療法剤などによって引き起こされるます。この修復が異常になると細胞死や細胞のがん化を引き起こします。
注4. クロマチンとは、真核生物の細胞の核内に存在するDNAとタンパク質からなる構造体で、染色質とも呼ばれています。遺伝子の発現を調節するなど、生命の活動に重要な役割を果たしています。
注5. クロマチンリモデリングとは、クロマチン(真核生物の細胞核内に存在するDNAとタンパク質の複合体)の構造を動的に調節することで、遺伝子発現(転写)やDNA修復やDNA複製を制御する仕組みです
注6. ゲノム安定性とは、ゲノムの変異や異常が起きない状態を指します。
論文情報
タイトル:Armadillo domain of ARID1A directly int er acts with DNA-PKcs to couple chromatin remodeling with nonhomologous end joining (NHEJ) pathway著者:Shin-ichiro Kanno, Takayasu Kobayashi, Reiko Watanabe, Akihiro Kurimasa, Kozo Tanaka, Akira Yasui, and Ayako Ui*
*責任著者:東北大学加齢医学研究所 准教授 宇井彩子
掲載誌:Nucleic Acids Research
DOI:10.1093/nar/gkaf150
詳細(プレスリリース本文)

問い合わせ先
(研究に関すること)東北大学 加齢医学研究所
准教授 宇井彩子
TEL:022-717-8469
Email: ayako.ui.c7*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学加齢医学研究所広報情報室
TEL: 022-717-8443
Email: ida-pr-office*grp.tohoku.ac.jp(*を@に置き換えてください)


東北大学は持続可能な開発目標(SDGs)を支援しています
 東北大学 研究
東北大学 研究